
| 气体 | 烧瓶和气体的总质量(g) |
| A | 48.4082 |
| B | 48.4082 |
| C | 48.4082 |
| D | 48.4342 |
| E | 48.8762 |
| V |
| Vm |
| V |
| Vm |
| V |
| Vm |
| 0.293L |
| 22.4L/mol |
| 0.293L |
| 22.4L/mol |
| 0.293L |
| 22.4L/mol |
| 1.12L |
| 22.4L/mol |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
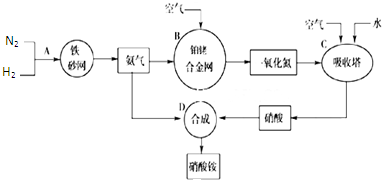
| ||
| △ |
| 注意事项 | 理由 | |
| ① | ||
| ② |
查看答案和解析>>
科目:高中化学 来源: 题型:
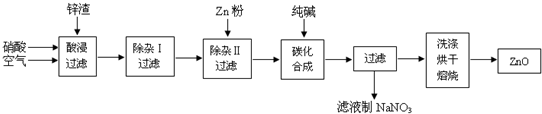
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
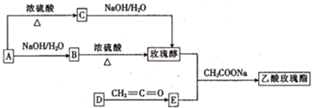
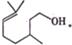

查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).则滴管和烧瓶中所用试剂不可能是( )
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体积对气球的影响).则滴管和烧瓶中所用试剂不可能是( )| 甲 | 乙 | |
| A | 水和过氧化钠 | 盐酸和NH3 |
| B | 双氧水和MnO2 | 水和NO |
| C | 盐酸和NaHCO3固体 | NaOH溶液和Cl2 |
| D | 饱和食盐水和电石 | 酸性高锰酸钾溶液和SO2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验方案 | 使用试剂 | 判断方法 |
| ① | 铁粉 | 如果有气泡,表明盐酸已经过量 |
| ② | pH试纸 | 如果pH<7,表明盐酸已经过量 |
| ③ | 硝酸银溶液 | 如果有白色沉淀产生,表明盐酸已经过量 |
| ④ | 紫色石蕊试液 | 如果溶液变成红色,表明盐酸已经过量 |
| A、① | B、② | C、③ | D、④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
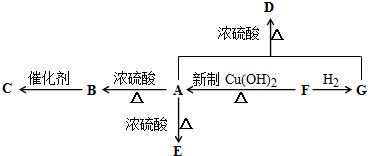
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com