
| A. | 标准状况下的22.4L辛烷完全燃烧,生成二氧化碳分子数为8NA | |
| B. | 1mol甲烷的质量与NA个甲烷分子的质量相等 | |
| C. | 28g氮气含有的原子数目为NA | |
| D. | 1mol碳正离子CH5+所含的电子总数为11NA |
分析 A、标况下辛烷为液态;
B、1mol甲烷中含NA个甲烷分子;
C、求出氮气的物质的量,然后根据1mol氮气中含2mol原子来分析;
D、CH5+中含10个电子.
解答 解:A、标况下辛烷为液态,故22.4L辛烷的物质的量不是1mol,故A错误;
B、1mol甲烷中含NA个甲烷分子,故1mol甲烷和NA个甲烷分子的质量相等,故B正确;
C、28g氮气的物质的量为1mol,而1mol氮气中含2mol原子即2NA个,故C错误;
D、CH5+中含10个电子,故1molCH5+中含10mol电子即10NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:解答题
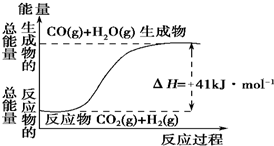 (1)根据如图所示情况,判断下列说法中正确的是B.
(1)根据如图所示情况,判断下列说法中正确的是B.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何反应都伴有能量的变化 | |
| B. | 化学反应中的能量变化可表现为热量的变化 | |
| C. | 反应物的总能量高于生成物的总能量时,发生吸热反应 | |
| D. | 反应物的总能量低于生成物的总能量时,发生吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a2<a1<197 | B. | 2a2>a1>197 | C. | 2a2=a1>197 | D. | 2a2=a1=197 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
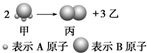 如图所示:已知甲、乙、丙常温下都为气体.2mol甲分子反应生成1mol丙和3mol乙,
如图所示:已知甲、乙、丙常温下都为气体.2mol甲分子反应生成1mol丙和3mol乙,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲烷中的氢原子被氯原子完全取代,需要2NACl | |
| B. | 1mol•L-1Mg(NO3)溶液中含有NO3-的数目为2NA | |
| C. | 标准状况下.22.4LBr2中所含的分子数为NA | |
| D. | Na2O2与水反应时,每生成0.1 molO2,转移电子的数目为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com