
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.086 | 0.102 | 0.074 |
| ��Ҫ���ϼ� | +2 | +3 | +2 | +6��-2 | -2 |
| A�� | L��M��R��T�γɵļ����ӵİ뾶������L | |
| B�� | �������Ũ�ȵ������ϡ���ᷴӦ������ΪQ��L | |
| C�� | ��̬�⻯���ȶ��ԣ�R��T | |
| D�� | M��T�γɵĻ����������ǿ�ᷴӦ������ǿ�Ӧ |
���� ������Ԫ�أ�T��R����-2�ۣ����ڢ�A�壬Tֻ��-2�ۣ���TΪOԪ�ء�RΪSԪ�أ�L��Q����+2�ۣ����ڢ�A�壬ԭ�Ӱ뾶L��Q����LΪMgԪ�ء�QΪBeԪ�أ�M��+3�ۣ����ڢ�A�壬ԭ�Ӱ뾶M�Ľ���L��R֮�䣬��MΪAlԪ�أ��Դ˽����⣮
��� �⣺�����Ϸ�����֪LΪMgԪ�ء�MΪAlԪ�ء�QΪBeԪ�ء�RΪSԪ�ء�TΪOԪ�أ�
A��L��M��R��T�γɵļ����ӵİ뾶������R�����Ӻ�����3�����Ӳ㣬��������2�����Ӳ㣬��A����
B��������Mg��Be��þ�����ᷴӦ��Ϊ���ң���B����
C���ǽ�����O��S��O��Ӧ���⻯����ȶ�����C����
D��M��T�γɵĻ�����Ϊ��������Ϊ���������������ǿ�ᷴӦ������ǿ�Ӧ����D��ȷ��
��ѡD��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã�Ϊ��Ƶ���㣬���ؿ���ѧ���ķ����������ؼ��Ǹ���ԭ�Ӱ뾶�����ϼ����ƶ�Ԫ�أ�ע���Ԫ�������ɵ����⣬��ϤԪ�ؼ��䵥�ʡ�����������ʣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢� | C�� | �ڢ� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ͷ�뵽�Ȼ�þ��Һ�У�2Na+Mg2+�TMg+2 Na+ | |
| B�� | �ѽ����Ʒ���ˮ�У�Na+2H2O�TNa++2OH-+H2�� | |
| C�� | ����ˮ����⻯����Һ�У�Cl2+2I-�T2Cl-+I2 | |
| D�� | �������ʯ��ʯ�ϣ�CO32-+2H+�TCO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼������Һ��ʯ����ķ�Ӧ��CO32-+Ca 2+=CaCO3�� | |
| B�� | ��������Һ��ʳ��ˮ�ķ���Ag++Cl-=AgCl�� | |
| C�� | п������ķ�Ӧ��Zn+2H++2Cl -=Zn 2++2Cl-+H2�� | |
| D�� | ���ˮ�еμ�FeCl3��Һ�Ʊ�Fe��OH��3���壺Fe 3++3H2O $\frac{\underline{\;\;��\;\;}}{\;}$ Fe��OH��3��+3H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʹ���ȱ�����Һ�У�Na+��Cl-��CH3 COO-��Fe2+ | |
| B�� | �������ܲ�������H2����Һ�У�Na+��NH4+��NO3-��Cl- | |
| C�� | ��ɫ��Һ�У�Al3+��NO3-��Cl-��SO42- | |
| D�� | c��FeCl3��=1.0mol/L����Һ�У�HCO3-��Cl-��H+��Na+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
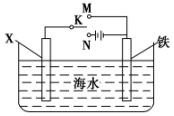 ������ͼװ�ã�����ģ�����ĵ绯ѧ������
������ͼװ�ã�����ģ�����ĵ绯ѧ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
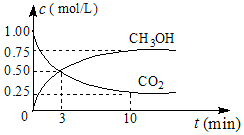 ��1���й�������ŵ����2020�꣬��λGDP������̼�ŷű�2005���½�40%��50%��
��1���й�������ŵ����2020�꣬��λGDP������̼�ŷű�2005���½�40%��50%��| �¶�/�� | 0 | 100 | 200 | 300 | 400 |
| ƽ�ⳣ�� | 667 | 13 | 1.9��10-2 | 2.4��10-4 | 1��10-5 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com