
 一种碳纳米管能够吸附氢气,用这种材料吸氢后制备的二次电池(充放电电池)工作原理如图所示,该电池的电解质为6mol•L-1KOH溶液,下列说法中正确的是( )
一种碳纳米管能够吸附氢气,用这种材料吸氢后制备的二次电池(充放电电池)工作原理如图所示,该电池的电解质为6mol•L-1KOH溶液,下列说法中正确的是( )| A. | 放电时K+移向碳电极 | |
| B. | 放电时电池负极的电极反应为H2-2e-═2H+ | |
| C. | 充电时镍电极的电极反应为:Ni(OH)2+OH--e-═NiO(OH)+H2O | |
| D. | 该电池充电时将碳电极与电源的正极相连,发生氧化反应 |
分析 A.放电时,电解质溶液中阳离子向正极移动;
B.放电时,负极上氢气失电子发生氧化反应;
C.电池充电时,镍电极做阳极,发生氧化反应;
D.该电池充电时,碳电极与电源的负极相连
解答 解:由图可知,充电时,电子流向碳电极,碳电极为阴极;镍电极是阳极.A.放电时,该电池为原电池,电解质溶液中阳离子向正极移动,所以钾离子向正极移动,故A错误;
B.放电时,负极上氢气失电子发生氧化反应,电极反应式为H2+2OH--2e-═2H2O,故B错误;C、充电时,镍电极作阳极,阳极上失电子发生氧化反应,电极反应式为Ni(OH)2-e-+OH-=NiO(OH)+H2O,故C正确;
D.充电时,碳纳米管电极作阴极,则与电源的负极相连,故D错误;
故选C.
点评 本题考查了原电池和电解池原理,明确正负极上发生的电极反应及阴阳离子的移动方向即可解答,易错选项是D,注意结合电解原理确定与原电池哪个电极相连,为易错点.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制的氯水保存在棕色广口瓶中,并放在阴凉处 | |
| B. | 用做感光片的溴化银贮存在无色试剂瓶中 | |
| C. | 烧碱溶液放在带磨口玻璃塞的试剂瓶中 | |
| D. | 1mol/L NaCl溶液不能长期保存在容量瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;镁条在气体B中燃烧生成的物质是Mg3N2(填化学式);
;镁条在气体B中燃烧生成的物质是Mg3N2(填化学式);查看答案和解析>>
科目:高中化学 来源: 题型:解答题
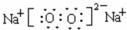 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.25mol•L-1 | B. | 0.50mol•L-1 | C. | 0.75mol•L-1 | D. | 1.25mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe与S混合加热生成FeS | |
| B. | Al箔在空气中受热可以熔化,由于氧化膜的存在,熔化的Al 并不滴落 | |
| C. | 检验SO2气体中是否含有CO2气体,可将气体先通入饱和碳酸氢钠溶液,再通入品红溶液,最后通入澄清石灰水溶液 | |
| D. | 氯化氢水溶液能导电,所以氯化氢是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热 溶解 过滤 结晶 | B. | 溶解 过滤 蒸发 结晶 | ||
| C. | 加热 溶解 蒸发 过滤 | D. | 溶解 过滤 蒸馏 蒸发 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com