
| A. | 在氧化还原反应中肯定有一种元素被氧化,另一种元素被还原 | |
| B. | 含有最高价元素的化合物不一定具有很强的氧化性 | |
| C. | 阳离子只能得到电子被还原,阴离子只能失去电子被氧化 | |
| D. | 化合反应和复分解反应不可能是氧化还原反应 |
分析 A.可能只有一种元素得到电子、也失去电子;
B、含有最高价元素的化合物,可能有强氧化性;
C.处于中间价态的微粒既有氧化性也有还原性;
D、有单质参加的化合反应和有单质生成的化合反应是氧化还原反应.
解答 解:A.可能只有一种元素得到电子、也失去电子,如氯气与水的反应中只有Cl元素的化合价变化,故A错误;
B.含有最高价元素的化合物,可能有强氧化性,如硝酸中N为最高价具有强氧化性,而二氧化碳中C为最高价不具有强氧化性,故B正确;
C.处于中间价态的微粒既有氧化性也有还原性,如亚铁离子、亚硫酸根离子等,故C错误;
D、有单质参加的化合反应和有单质生成的化合反应是氧化还原反应,所以化合反应和复分解反应可能是氧化还原反应,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及分析应用能力的考查,题目难度不大.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:实验题
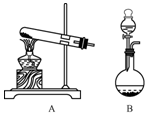 实验室制取氨气有几种方法.
实验室制取氨气有几种方法.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ② | C. | ③ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝铵与草木灰不能混合使用,否则将使前者失去肥效,而后者仍有肥效 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 可用于制作航天服的聚酯纤维是新型无机非金属材料 | |
| D. | 采用“静电除尘”、“原煤脱硫”、“汽车尾气催化净化”等方法,可提高空气质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为10的氧原子:810O | B. | 氧负离子(O2-)的结构示意图: | ||
| C. | Na2O2的电子式: | D. | 1-丙醇的结构简式: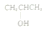 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A12O3属于两性氧化物 | |
| B. | 两步反应中CO均是氧化产物 | |
| C. | Al4C3与盐酸反应可生成烃,该烃为乙烯 | |
| D. | 生成的铝粉不能在空气中冷却 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com