
��8�֣���ѧ��һֱ�������о����¡���ѹ�¡��˹��̵������·���������ʵ�鱨�����ڳ��¡���ѹ�����������£�N2�ڴ�������������Fe2O3��TiO2��������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����һ���о�NH3���������¶ȵĹ�ϵ������ʵ�����ݼ��±������ա�N2ѹ��1.0��105Pa����Ӧʱ��3h����
|
T/K |
303 |
313 |
323 |
353 |
|
NH3������/��10-6mol�� |
4.8 |
5.9 |
6.0 |
2.0 |
��Ӧ���Ȼ�ѧ����ʽ���£�
N2��g��+3H2O��l��====2NH3��g��+ O2��g�� ��H=+765.2kJ��mol-1
O2��g�� ��H=+765.2kJ��mol-1
�ش��������⣺
��1����ͼ��������Ӧ����������·�Ӧ��������ϵ�����仯ʾ��ͼ������ͼ�л������д�������·�Ӧ��������ϵ�����仯ʾ��ͼ��

��2����Ŀǰ�㷺ʹ�õĹ�ҵ�ϳɰ�������ȣ��÷����й̵���Ӧ�������������������䷴Ӧ����������NH3�������Ľ��飺 ��
��3����ҵ�ϳɰ��ķ�ӦΪN2��g��+3H2��g�� 2NH3��g���������ݻ�Ϊ2.0L���ܱ������г���0.60molN2��g����1.60molH2��g������Ӧ��һ�������´ﵽƽ��ʱ��NH3�����ʵ���������NH2�����ʵ����뷴Ӧ��ϵ���ܵ����ʵ���֮�ȣ�Ϊ
2NH3��g���������ݻ�Ϊ2.0L���ܱ������г���0.60molN2��g����1.60molH2��g������Ӧ��һ�������´ﵽƽ��ʱ��NH3�����ʵ���������NH2�����ʵ����뷴Ӧ��ϵ���ܵ����ʵ���֮�ȣ�Ϊ ������
������
�ٸ�������N2��ƽ��ת������ ��
�ڸ������·�Ӧ2NH3��g�� N2��g��+3H2��g����ƽ�ⳣ��Ϊ
��
N2��g��+3H2��g����ƽ�ⳣ��Ϊ
��
�����¶Ȳ��䣬��С�����������ƽ����---------------------------�ƶ���c(NH3)��--------------------
c(N2)��---------------------- ��������С�䣩
��1����ͼ�ԡ���2�֣�
��2�������¶ȣ�����Ӧ��N2��Ũ�ȣ������Ƴ�������(2��)
��3��66.7%��2�֣�?0.005��2�֣�
����������1����ͼҪ�㣺�ٴ����ɽ��ͷ�Ӧ�Ļ�ܣ�����Ը���Ӧǰ�������仯���������κ�Ӱ�졣
�ڸ÷�ӦΪ���ȷ�Ӧ�����Է�Ӧ���������Ҫ�������������������
��2���÷�Ӧ������Ӧ�����ȷ�Ӧ�������¶ȣ�ʹ��ѧƽ��������Ӧ�����ƶ����Ӷ�����NH3���������������¶�Ҳ����߷�Ӧ���ʣ�����Ӧ��N2��Ũ�ȣ��ӿ췴Ӧ���ʣ���ʹ��ѧƽ�������ƶ��������Ƴ������ʹƽ�������ƶ�������NH3����������
��3��������ʽ�������֪����ʼʱ��c��N2��=0.3mol��L-1��ƽ��ʱ��c��N2��=0.1 mol��L-1;?c��H2��=0.2 mol��L-1;c��NH3��=0.4 mol��L-1��
������N2��ƽ��ת���� ��
��
��
��Ӧ2NH3��g��====N2��g��+3H2��g����ƽ�ⳣ��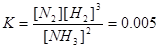 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| T/K | 303 | 313 | 323 |
| ƽ��ʱNH3��������/��10-6mol�� | 4.8 | 5.9 | 6.0 |
| ||
| ||


| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| T/K | 303 | 313 | 323 | 353 |
| NH3������/��10-6mol�� | 4.8 | 5.9 | 6.0 | 2.0 |
| 3 |
| 2 |
 2NH3��g���������ݻ�Ϊ2.0L���ܱ������г���0.60mol N2��g����1.60molH2��g������Ӧ��һ�������´ﵽƽ��ʱ��NH3�����ʵ���������NH3�����ʵ����뷴Ӧ��ϵ���ܵ����ʵ���֮�ȣ�Ϊ
2NH3��g���������ݻ�Ϊ2.0L���ܱ������г���0.60mol N2��g����1.60molH2��g������Ӧ��һ�������´ﵽƽ��ʱ��NH3�����ʵ���������NH3�����ʵ����뷴Ӧ��ϵ���ܵ����ʵ���֮�ȣ�Ϊ| 4 |
| 7 |
 N2��g��+3H2��g����ƽ�ⳣ����
N2��g��+3H2��g����ƽ�ⳣ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��Ȼ���ﵪ�Ĺ̶�;��֮һ��������������£�N2��O2��Ӧ����NO��
��Ȼ���ﵪ�Ĺ̶�;��֮һ��������������£�N2��O2��Ӧ����NO��| �¶�/�� | 1538 | 1760 | 2404 |
| ƽ�ⳣ��K | 0.86��10-4 | 2.6��10-4 | 64��10-4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| T/K | 303 | 313 | 323 | 353 |
| NH3������/��10-6 mol�� | 4.8 | 5.9 | 6.0 | 2.0 |
| 3 |
| 2 |
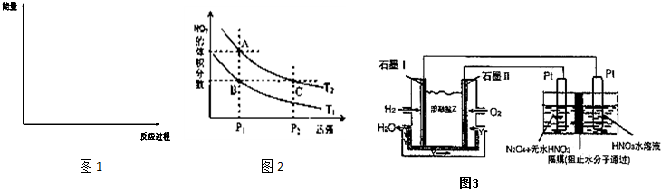
| 4 |
| 7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012�갲�պ����а������и߶���ѧ�������������ƻ�ѧ�Ծ����������� ���ͣ������
��6�֣���Ȼ���ﵪ�Ĺ̶�;��֮һ��������������£�N2��O2��Ӧ����NO��
��1���ڲ�ͬ�¶��£���ӦN2(g)��O2(g) 2NO(g) DH��a kJ��mol��1��ƽ�ⳣ��K���±���
2NO(g) DH��a kJ��mol��1��ƽ�ⳣ��K���±���
| �¶�/�� | 1538 | 1760 | 2404 |
| ƽ�ⳣ��K | 0.86��10��4 | 2.6��10��4 | 64��10��4 |
 2NO(g)�ﵽƽ��ʱN2��Ũ��Ϊ �������¶��²�����O2��NO�ķ�Ӧ��������������λ��Ч���֣�
2NO(g)�ﵽƽ��ʱN2��Ũ��Ϊ �������¶��²�����O2��NO�ķ�Ӧ��������������λ��Ч���֣��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com