
【题目】天门冬氨酸锌是一种补锌剂,可以![]() 、天门冬氨酸(
、天门冬氨酸(![]() )为原料制备。回答下列问题:
)为原料制备。回答下列问题:
(1)Zn成为阳离子时首先失去______轨道电子。碲(Te)与O同主族,则Te元素中电子占据的能量最高的能级是______。
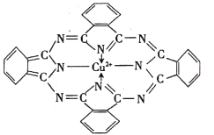
(2)P是N的同族元素,PH3与NH3中稳定性更高的是______(填化学式),其判断理由是______;酞菁铜可用于生产蓝色颜料(结构如图),其中C原子的轨道杂化类型为______。
(3)CO为______(填“极性”或“非极性”)分子。
(4)ZnO晶体的一种晶胞结构如图:
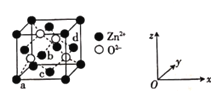
①![]() 的配位数为____________。
的配位数为____________。
②以晶胞边长为单位长度建立的坐标系可表示晶胞中锌原子的位置,称作原子分数坐标。图中原子a的分数坐标为![]() ,原子d的分数坐标为
,原子d的分数坐标为![]() ,则原子b和c的分数坐标分别为______、______。
,则原子b和c的分数坐标分别为______、______。
③设![]() 为阿伏加德罗常数的值。已知晶胞边长为
为阿伏加德罗常数的值。已知晶胞边长为![]() nm,则ZnO晶体的密度为______(列出计算式)
nm,则ZnO晶体的密度为______(列出计算式)![]() 。
。
【答案】4s 5p ![]() N原子半径更小,N-H键的键长更短,键能更大,故NH3更稳定 sp2 极性 4
N原子半径更小,N-H键的键长更短,键能更大,故NH3更稳定 sp2 极性 4 ![]()
![]()
![]()
【解析】
(1)根据原子的核外电子排布分析;
(2)根据分子的结构特点分析;根据杂化轨道理论分析
(4)根据配位数的概念和晶胞结构特点分析计算。
(1)Zn为65号元素,其价电子排布式为[Ar]3d104s2,其成为阳离子时首先失去4s轨道电子;碲(Te)与O同主族,其位于第五周期第VIA族,其价电子排布式为5s25p4,则Te元素中电子占据的能量最高的能级是5p;
(2)P是N的同族元素,由于N原子半径更小,N-H键的键长更短,键能更大,故NH3更稳定;酞菁铜中C原子均形成3个σ键,无孤电子对,故价层电子对数均为3,则C原子的的轨道杂化类型为sp2;
(3)CO为碳原子与氧原子间形成极性键的双原子分子,故其为极性分子;
(4)①由图可知,与![]() 距离最近且相等的Zn2+的个数为4,故其配位数为4;
距离最近且相等的Zn2+的个数为4,故其配位数为4;
②由图可知,原子b的坐标为![]() ,c的坐标为
,c的坐标为![]() ;
;
③由图可知,一个晶胞中![]() 的个数为4,Zn2+的个数为
的个数为4,Zn2+的个数为![]() ,则ZnO晶体的密度为
,则ZnO晶体的密度为![]() 。
。


 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数为NA。关于 l00mLl mol/L的Fe2(SO4)3溶液,下列说法正确是
A.加NaOH可制得Fe(OH)3 胶粒0.2NA
B.溶液中阳离子数目为0.2NA
C.加Na2CO3 溶液发生的反应为 3CO32-+ 2Fe3+ = Fe2(CO3 )3↓
D.Fe2(SO4)3溶液可用于净化水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置做下面的实验:在烧杯中盛有半杯乙溶液,然后用滴定管向容器中滴入甲溶液。随着甲的滴入,灯泡逐渐变暗;滴到一定量时,灯泡熄灭,继续滴入甲溶液,灯泡又逐渐变亮。下列各组溶液中,能够产生上述现象的是 ( )
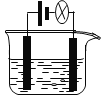
选项 | 甲 | 乙 |
A | NH3·H2O | HCl |
B | CH3COOH | NH3·H2O |
C | NaOH | MgCl2 |
D | H2SO4 | Ba(OH)2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各溶液中,离子一定能大量共存的是( )
A.使甲基橙试液变红的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
B.常温下,![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
C.溶质为![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
D.水电离出的![]() 的溶液:
的溶液:![]() 、
、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作与现象相匹配的是( )
选项 | 实验操作 | 现象 |
A | 将石蜡油分解得到的产物直接通入少量溴的CCl4溶液中 | 无明显现象 |
B | 将浓硫酸和蔗糖反应产生的气体通入少量的 | 气体全部被吸收且溶液紫红色变浅 |
C | 向淀粉碘化钾溶液中通入过量氯气 | 溶液先变蓝后褪色 |
D | 向 | 无沉淀生成 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列反应的化学方程式:
(1)丙烯制备聚丙烯:______;
(2)2-甲基-1,3-丁二烯与Br2的1,4-加成反应______;
(3)1,2-二溴乙烷在氢氧化钠、乙醇中加热______;
(4)实验室制备乙炔气体:______;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为短周期主族元素,它们的最高正化合价和原子半径如下表所示:
元素 | X | Y | Z | W |
最高正化合价 | +3 | +1 | +5 | +7 |
原子半径 | 0.082 | 0.186 | 0.110 | 0.099 |
则下列说法错误的是
A.X的最高价氧化物对应的水化物具有两性
B.ZW3分子中所有原子最外层均满足8e-结构
C.Y的一种氧化物可用作供氧剂,Z的一种氧化物可用作干燥剂
D.简单气态氢化物的热稳定性:W>Z>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)写出![]() 与
与![]() 反应的化学方程式________。
反应的化学方程式________。
(2)能一次鉴别出苯、苯酚、已烯、氯仿的试剂是________。
(3)写出皂化反应的化学方程式________。
(4)写出蔗糖水解的化学方程式________。
(5)酚醛树脂的结构简式为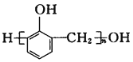 ,写出其单体的结构简式________。
,写出其单体的结构简式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸工厂运用电化学原理设计了如图所示的装置,实现了用SO2发电的同时制备硫酸。图中电极是含催化剂、多孔吸附性的惰性材料。下列说法正确的是
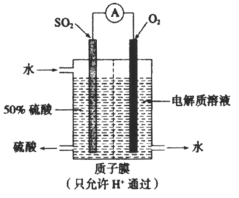
A.通入SO2气体的一极是负极,发生还原反应
B.正极的电极反应:O2+4e=2O2
C.该装置工作时的总反应:2SO2+O2+2H2O=2H2SO4
D.氢离子向负极区移动,与负极生成的SO42结合形成硫酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com