
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列条件关于离子共存说法中正确的是
| A.d点对应的溶液中大量存在:Na+、K+、SO32—、Cl— |
| B.b点对应的溶液中大量存在:NH4+、Ba2+、OH-、I- |
| C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、CO32- |
| D.a点对应的溶液中大量存在:Fe3+、Na+、Cl-、SO42— |
A
解析试题分析:离子间如果发生化学反应,则不能大量共存,反之是可以的。根据水的离子积常数和图像可知,d点溶液显碱性,可以大量共存,A正确;b点溶液显酸性,OH-不能大量共存,且B中NH和OH-不能大量共存;c点溶液显中性,但Ba2+和CO32-不能大量共存;a点溶液显中性,铁离子不能大量共存,答案选A。
考点:考查离子共存的正误判断
点评:离子不能大量共存的一般情况是:(1)能发生复分解反应的离子之间(即生成沉淀,气体,水、弱酸、弱碱等难电离物质);(2)能生成难溶物的离子之间(如:Ca2+和 SO42-;Ag+和 SO42-);(3)能完全水解的离子之间,如多元弱酸和弱碱盐的阴、阳离子(如:Al3+, Fe3+与 CO32-、HCO3-、AlO2-等);(4)能发生氧化还原反应的离子之间(如:Fe 、H+、NO3-;S2-、ClO-;S2-、 Fe3+等);(5)能发生络合反应的离子之间(如 Fe3+和 SCN-);解决离子共存问题时还应该注意题目所隐含的条件,题目所隐含的条件一般有:(1)溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;(2)溶液的颜色,如无色时可排除 Cu2+、 Fe2+、Fe3+、MnO4-等有色离子的存在;(3)溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;(4)是“可能”共存,还是“一定”共存等。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
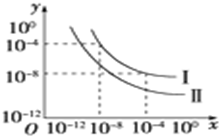 在不同温度下的水溶液中c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示.请回答下列问题:
在不同温度下的水溶液中c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y的关系如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
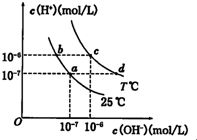 在不同温度下.水溶液中c(H+)与c(OH+)有如图所示的关系,下列说法中不正确的是( )
在不同温度下.水溶液中c(H+)与c(OH+)有如图所示的关系,下列说法中不正确的是( )| A、图中T>25 | B、b点溶液c(H+)一定比a点大 | C、c点对应的洛液中可能大量存在Al3+、Cl- | D、d点对应的溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
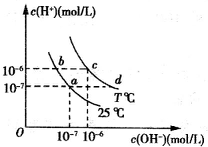 在不同温度下,水溶液中c(H+)与c(OH-)的关系如图所示.下列有关说法中正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)的关系如图所示.下列有关说法中正确的是( )| A、若从a点到c点,可采用在水中加入酸的方法 | B、b点对应的醋酸中由水电离的c(H+)=10-6mol/L | C、c点对应溶液的Kw大于d点对应溶液的Kw | D、T℃时,0.05 mol?L-1的Ba(OH)2溶液的pH=11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
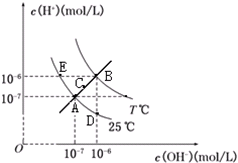 在不同温度下,水溶液中c(H+)与c(OH-)关系如图所示.下列说法不正确的是( )
在不同温度下,水溶液中c(H+)与c(OH-)关系如图所示.下列说法不正确的是( )| A、图中五点Kw间的关系:B>C>A=D=E | B、E点对应的水溶液中,可能有NH4+、Ba2+、Cl-、I-大量同时存在 | C、若处在B点时,将pH=2的硫酸溶液与pH=10的KOH溶液等体积混合,所得溶液呈中性 | D、若0.1 mol/L的NaHA溶液水溶液中c(H+)与c(OH-)关系如图D点所示,则溶液中有:c(HA-)>c(OH-)>c(A2-)>c(H2A) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com