
下列物质中属于高分子化合物的是( )
①淀粉 ②纤维素 ③氨基酸 ④油脂 ⑤蔗糖 ⑥酚醛树脂 ⑦聚乙烯 ⑧蛋白质
A.①②③⑦⑧ B.①④⑥⑦
C.①②⑥⑦⑧ D.②③④⑥⑦⑧
科目:高中化学 来源: 题型:
有反应mA(g)+nB(g) 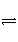
 wC(g),测得在同一时间 内A每分钟减少0.15 mol·L- 1, B每分钟减少0.05 mol·L-1,C每分钟增加0.1 mol·L- 1,则下列叙述不正确的是( )
wC(g),测得在同一时间 内A每分钟减少0.15 mol·L- 1, B每分钟减少0.05 mol·L-1,C每分钟增加0.1 mol·L- 1,则下列叙述不正确的是( )
A.m∶n∶w=3∶1∶2
B.体积和温度不变时,若在前10s内A减少了x mol,则在前20s内减少小于2x mol
C.体积和温度不变时,随反应进行压强逐渐下降,一段时间后压强保持恒定不变
D.单位时间内反应物浓度的减少等于生成物浓度的增加
查看答案和解析>>
科目:高中化学 来源: 题型:
向某溶液中滴加KSCN的溶液,无明显现象,再向其中滴加氯水,溶液变为血红色,则下列说法正确的是( )
A.原溶液中一定含有Fe3+离子 ,不含Fe2+
B.溶液中的Fe2+ 离子被氯气还原为Fe3+
C.原溶液中一定含有Fe2+ 离子 ,不含Fe3+
D.溶液中同时含Fe2+ 或Fe3+离子
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是探究铁发生腐蚀的装置图。发现开始时U形管左端红墨水水柱下降,一段时间后U形管左端红墨水水柱又上升。下列说法中不正确的是
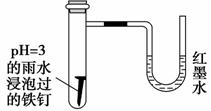
A.开始时发生的是析氢腐蚀
B.一段时间后发生的是吸氧腐蚀
C.两种腐蚀负极的电极反应式均为 Fe-2e-===Fe2+
D.析氢腐蚀的总反应式为 2Fe+O2+2H2O===2Fe(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
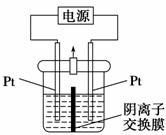 电解装置如右图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知:3I2+6OH-===IO
电解装置如右图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。已知:3I2+6OH-===IO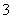 +5I-+3H2O
+5I-+3H2O
下列说法不正确的是
A.右侧发生的电极反应式:2H2O+2e-===H2↑+2OH-
B.电解结束时,右侧溶液中含有IO
C.电解槽内发生反应的总化学方程式:KI+3H2O KIO3+3H2↑
KIO3+3H2↑
D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学反应不变
查看答案和解析>>
科目:高中化学 来源: 题型:
某高分子化合物的部分结构如下:

关于该物质的下列说法中,正确的是( )
A.聚合物的链节为
B.聚合物的分子式为C3H3Cl3
C.合成该聚合物的单体是CHCl===CHCl
D.若n为链节数,则其相对 分子质量为97n
分子质量为97n
查看答案和解析>>
科目:高中化学 来源: 题型:
合成P(一种抗氧化剂)的路线如下:

②A和F互为同分异构体,A分子中有三个甲基,F分子中只有一个甲基。
(1)A→B的反应类型为____________。B经催化加氢生成G(C4H10),G的化学名称是____________________________________。
(2)A与浓HBr溶液一起共热生成H,H的结构简式为
____________________________________。
(3)实验室中检验C可选择下列试剂中的________。
a.盐酸 B.FeCl3溶液
c.NaHCO3溶液 D.浓溴水
(4)P与足量NaOH溶液反应的化学反应方程式为_____________________________
____________________________________(有机物用结构简式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个容积固定为2 L的密闭容器中,发生反应aA(g)+bB(g)pC(g) ΔH=?,反应情况记录如表:
| 时间 | c(A) (mol·L-1) | c(B) (mol·L-1) | c(C) (mol·L-1) |
| 0 | 1 | 3 | 0 |
| 第2 min[ | 0.8[ | 2.6 | 0.4 |
| 第4 min | 0.4 | 1.8 | 1.2 |
| 第6 min | 0.4 | 1.8 | 1.2 |
请仔细分析,根据表中数据,回答下列问题:
(1)a=________,b=________,p=________。(取最小正整数)
(2)第2 min到第4 min内A的平均反应速率v(A)=________ mol·L-1·min-1。
(3)若从开始到第4 min建立平衡时反应放出的热量为235.92 kJ,则该反应的ΔH=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com