
过量的NaHCO3和Na2O2混合,在密闭容器中充分混合加热后,最后排出气体,残留的固体是( )
A.Na2O B.Na2O2和Na2CO3
C.Na2CO3 D.Na2O2和Na2O
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
Na2O2、HCl、Al2O3 三种物质在水中完全反应后,溶液中只含有Na+、H+、Cl﹣、OH﹣;且溶液呈中性,则Na2O2、HCl、Al2O3的物质的量之比可能为( )
|
| A. | 3:2:1 | B. | 2:4:1 | C. | 2:3:1 | D. | 4:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Mg2+、Al3+等离子。当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀物质的量随盐酸的体积变化如下图所示。由此可知原溶液中
A.不含SO42-
B.含有的阴离子一定是OH-、AlO2-、SiO32-
C.含有的阴离子一定是OH-、CO32-、AlO2-、SiO32-
D.含有AlO2-与SiO32-的物质的量之比为3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体
 积的关系如右图所示,由此确定,原溶液中含有的阳离子是( )
积的关系如右图所示,由此确定,原溶液中含有的阳离子是( )
A.Mg2+、Al3+、Fe2+
B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+
D.只有Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
聚丙烯酸酯的结构为━[ CH2-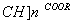 ,下列有关它的说法中,不正确的是
,下列有关它的说法中,不正确的是
A.它可由CH2=CH-COOR经加成聚合反应得到
B.在一定条件下能发生加成反应
C.聚丙烯酸酯材料是一种混合物
D.聚丙烯酸酯是高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.金属单质与盐溶液的反应都是置换反应
B.4Fe(OH)2+O2+2H2O===4Fe(OH)3属于化合反应
C.SO2+Cl2+2H2O===2HCl+H2SO4属于氧化还原反应
D.反应AgNO3+HCl===AgCl↓+HNO3不能说明盐酸酸性比硝酸强
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
①高铁电池的负极材料是________。
②放电时,正极发生________(填“氧化”或“还原”)
反应:已知负极反应为Zn-2e-+2OH-===Zn(OH)2,则正极反应为________________________________________________________________。
③放电时,________(填“正”或“负”)极附近溶液的碱性增强。
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
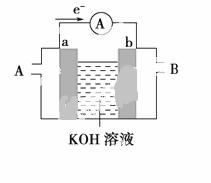
①使用时,空气从________口通入(填“A”或“B”);
②假设使用的“燃料”是甲醇,a极的电极反应式为_______________________________________;
③假设使用的“燃料”是水煤气(成分为CO、H2),如用这种电池电镀铜,待镀金属的质量增加6.4 g,则至少消耗标准状况下水煤气的体积为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com