
| A. | H3PO4 | B. | Na3PO4 | C. | Ag | D. | Na2HPO2 |
分析 NaH2PO2为正盐,可将溶液中的Ag+还原为Ag,Ag元素的化合价降低,P元素的化合价升高,结合氧化剂与还原剂的物质的量之比为4:1及电子守恒计算.
解答 解:NaH2PO2为正盐,可将溶液中的Ag+还原为Ag,Ag元素的化合价降低,P元素的化合价升高,
设氧化产物中P元素的化合价为x,
由氧化剂与还原剂的物质的量之比为4:1及电子守恒可知,
4×(1-0)=1×(x-1),
解得x=+5,
由H3PO2+4Ag++2H2O=H3PO4+4Ag+4H+,
H2PO2-+4Ag++2H2O=H3PO4+4Ag+3H+,
则NaH2PO2对应的氧化产物为H3PO4,
故选A.
点评 本题考查氧化还原反应的计算,为高频考点,把握反应中元素的化合价变化、电子守恒为解答的关键,侧重分析与计算能力的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:推断题
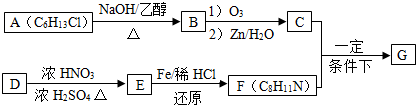
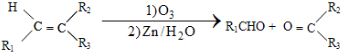
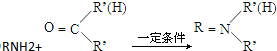
 +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$  +H2O;
+H2O; ;
; ,(写出其中的一种的结构简式).
,(写出其中的一种的结构简式).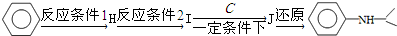
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合前醋酸溶液中水的电离程度大 | |
| B. | 混合前c(CH3COOH)大于c(Na+) | |
| C. | 混合后若c(Na+)=c(CH3COO-),则混合前乙酸体积大 | |
| D. | 分别稀释10倍,两溶液的pH之和大于14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核外电子数为86 | B. | 中子数为86 | C. | 质子数为136 | D. | 核电荷数为222 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
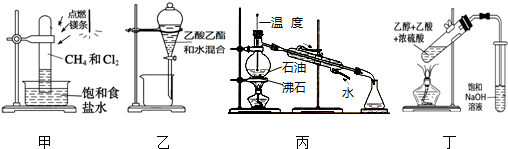
| A. | 用装置甲在强光照条件下制取一氯甲烷 | |
| B. | 用装置乙分离乙酸乙酯和水 | |
| C. | 用装置丙蒸馏石油并收集60~150℃馏分 | |
| D. | 用装置丁制取并收集乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用稀Na0H溶液除去乙酸乙酯中的乙酸 | |
| B. | 一定条件下可以用H2除去乙烷中混有的乙烯 | |
| C. | 蒸馏时温度计的水银球应插入液面之下 | |
| D. | 酸碱中和滴定实验中,锥形瓶用蒸馏水洗涤后,即可注入待测液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 消耗B 0.08mol | B. | x=2 | ||
| C. | A的平衡浓度是1.4mol/L | D. | 平衡时气体压强是原来的0.94倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
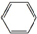 .
. ,取代反应.
,取代反应.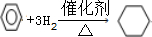 ,加成反应.
,加成反应.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 已知下列数据:
已知下列数据:| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) |
| 乙醇 | -117.0 | 78.0 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸(98%) | - | 338.0 | 1.84 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com