
 过氧化氢和臭氧是用途很广的氧化剂.试回答下列问题:
过氧化氢和臭氧是用途很广的氧化剂.试回答下列问题: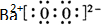 (写电子式),
(写电子式),分析 (1)酸性条件下H2O2氧化KI生成碘单质和水;
(2)根据题目信息,实验室通过上述某种过氧化物与适量稀硫酸作用,过滤后即可制得较纯净的H2O2溶液,说明生成了沉淀;
(3)N2H4(l)+O2(g)═N2(g)+2H2O(g),△H=-534kJ•mol-1①
H2O2(l)=H2O(l)+$\frac{1}{2}$O2(g)△H=-98.64kJ mol-1②
H2O(l)═H2O(g),△H=+44kJ•mol-1③
根据盖斯定律,将①+2②+4③计算;
(4)①反应中碘化钾是还原剂,臭氧作氧化剂得电子发生还原反应,反应中得电子化合价降低的物质是氧化剂,氧化剂对应的产物是还原产物;
②依据元素化合价变化结合电子守恒配平书写化学方程式;
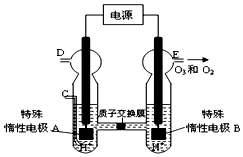
(5)①由图可知,B极生成O2、O3,B极反应氧化反应,电解池阳极发生氧化反应,故A为阴极;
②若C处不通入O2,实质为电解水,D处为氢气,体积为11.2L,E处为氧气、臭氧,体积共为4.48L,令臭氧的体积为xL,利用电子转移守恒列放出计算x的值,再根据体积分数定义计算;
③C处通入O2,O2发生还原反应,在酸性条件下生成水.
解答 解:(1)酸性条件下H2O2氧化KI生成碘单质和水,反应的离子方程式为:H2O2+2I-+2H+═I2+2H2O;
故答案为:H2O2+2I-+2H+═I2+2H2O;
(2)实验室通过上述某种过氧化物与适量稀硫酸作用,过滤后即可制得较纯净的H2O2溶液,说明生成了硫酸钡沉淀,所以选用BaO2,过氧化钡是离子化合物,电子式为: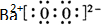 故答案为:
故答案为: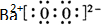 ;
;
(3)N2H4(l)+O2(g)═N2(g)+2H2O(g),△H=-534kJ•mol-1①
H2O2(l)=H2O(l)+$\frac{1}{2}$O2(g)△H=-98.64kJ mol-1②
H2O(l)═H2O(g),△H=+44kJ•mol-1③
将①+2②+4③可得:N2H4(l)+2H2O2(l)=N2(g)+4H2O(g)△H=(-534kJ•mol-1)+2×(-98.64kJ•mol-1)+4×(+44kJ•mol-1)=-643.28 kJ•mol-1
故答案为:-643.28 kJ•mol-1;
(4)该反应中臭氧得电子化合价降低,所以臭氧是氧化剂;氧化剂对应的产物是还原产物,所以氢氧化钾是还原产物,碘元素化合价-1价变化为0价,氧元素化合价变化为-2价,结合电子守恒配平书写化学方程式为:2KI+O3+H2O=2KOH+I2+O2;
故答案为:KOH;2KI+O3+H2O=2KOH+I2+O2;
(5)①由图可知,B极生成O2、O3,B极反应氧化反应,电解池阳极发生氧化反应,故A为阴极,电极反应为2H++2e-═H2↑,故答案为:A;
②若C处不通入O2,实质为电解水,D处为氢气,体积为11.2 L,物质的量为0.5mol,E处为氧气、臭氧,体积共为4.48L,物质的量为0.2mol;
令臭氧的体积为xL,根据电子转移守恒有
0.5×2=x×3×2+(0.2-x)×2×2,解得Z=0.5mol-2×0.2mol=0.1,所以E处收集的气体中O3所占的体积分数为$\frac{0.1mol}{0.2mol}$×100%=50%,
故答案为:50%;
③C处通入O2,O2发生还原反应,在酸性条件下生成水,电极反应式为O2+4H++4e-=2H2O,故答案为:O2+4H++4e-=2H2O.
点评 本题考查原电池与电解池反应原理、反应热的计算、氧化还原反应计算、化学平衡图象、阅读题目获取信息的能力等,难度中等,需要学生具备运用信息与基础知识分析问题、解决问题的能力.


 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源:2016-2017学年山东省德州市高二上10月月考化学试卷(解析版) 题型:填空题
已知可逆反应:M(g)+N(g)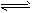 P(g)+Q(g),△H>0请回答下列问题:
P(g)+Q(g),△H>0请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)= 1 mol·L-1,c(N)=2.4 mol·L-1,达到平衡后,M的转化率为60%,此时N的转化率为_____________;
(2)若反应在相同条件下进行达到平衡后,再向容器中充入M气体,再次达到平衡时该反应的平衡常数K_________(填“增大”“减小”或“不变”下同)。
(3)若反应温度不变,反应物的起始浓度分别为:c(M)= 4mol·L-1, c(N)=a mol·L-1,达到平衡后,c(P)=2 mol·L-1,则a=_________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省徐州市高一上第一次月考化学卷(解析版) 题型:选择题
14C的放射性可用于考古断代。下列关于14C的说法中正确的是
A. 质量数为6 B. 质子数为6 C. 电子数为14 D. 中子数为14
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 周期表中第15纵行(从左往右数)元素的最高正价为+5 | |
| B. | 元素周期表中位于金属和非金属非界线附近的元素属于过渡元素 | |
| C. | 离子化合物中可能含有共价键,共价化合物中可能含有离子键 | |
| D. | 同一主族的甲乙两种元素,甲的原子序数为a,则乙的原子序数可能为a+4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1(b-2a)mol/L | B. | 0.4( 2a-b)mol/L | C. | 10(b-2a)mol/L | D. | 4(b-2a)mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气是一种黄绿色有毒气体,密度比空气大 | |
| B. | 氯气常用于制备漂白粉等杀菌消毒剂 | |
| C. | 新制氯水具有漂白作用,是因为Cl2具有强氧化性 | |
| D. | 氯元素在自然界中以化合态存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
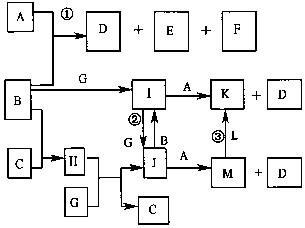 如图是部分元素的单质及其化合物的转化关系图(有关反应的条件己略去);己知:B、C、G、L 均为单质,其中在常温、常压下,G是固体,B、C、L是气体;生成物E具有漂白性,且焰色反应呈黄色;F 在常温下是液体;K、M 均为不溶于水的沉淀,其中K 为红褐色.
如图是部分元素的单质及其化合物的转化关系图(有关反应的条件己略去);己知:B、C、G、L 均为单质,其中在常温、常压下,G是固体,B、C、L是气体;生成物E具有漂白性,且焰色反应呈黄色;F 在常温下是液体;K、M 均为不溶于水的沉淀,其中K 为红褐色. ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
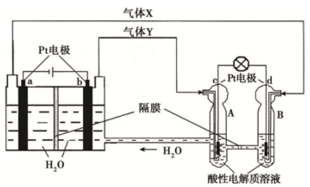 (1)某蓄电池的反应为NiO2+Fe+2H2O $?_{充电}^{放电}$Fe(OH)2+Ni(OH)2.
(1)某蓄电池的反应为NiO2+Fe+2H2O $?_{充电}^{放电}$Fe(OH)2+Ni(OH)2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com