
【题目】利用固体表面催化工艺进行NO分解的过程如图所示(![]() N
N![]() O)。下列说法不正确的是( )
O)。下列说法不正确的是( )
![]()
A.NO属于极性分子
B.含有非极性共价键
C.过程②释放能量,过程③吸收能量
D.标准状况下,NO分解生成5.6LN2转移电子数为6.02×1023
【答案】C
【解析】
分析NO分解的过程,可知过程①为固体表面吸附NO分子的过程,过程②中发生了旧化学键的断裂:2NO=2N+2O;过程③为新化学键的形成过程:2N=N2、2O=O2。过程④为解吸过程,据此进行分析。
A.NO中存在极性键,其空间结构不对称,键的极性不能抵消,故NO为极性分子,A项正确;
B.在N2、O2中存在非极性共价键,B项正确;
C.过程②为化学键断裂过程,吸收能量,过程③为新化学键的形成,会释放能量,C项错误;
D.NO分解成1molN2的过程中,转移了4mole-,标准状况下,5.6LN2的物质的量为0.25mol,则生成0.25molN2的过程中,转移的电子数为6.02×1023,D项正确;
答案选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产、生活中有着广泛的应用。
(1)基态Fe原子中,电子填充的能量最高的能级符号为__。
(2)在空气中FeO稳定性小于Fe2O3,从电子排布的角度分析,其主要原因是__。
(3)铁氰化钾{K3[Fe(CN)6])}溶液是检验Fe2+常用的试剂。lmol[Fe(CN)6]3-含σ键的数目为__。
(4)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是__。配体N3-中心原子的杂化类型为__。CoO的熔点是1935℃,CoS的熔点是1135℃,试分析CoO的熔点较高的原因__。
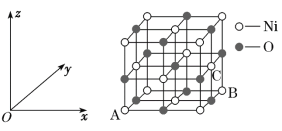
(5)NiO的晶胞结构如图所示,其中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸埃洛替尼(I)是一种抑制癌细胞增殖的药物,其合成路线如图:

已知:

(l)下列说法不正确的是___。
A.上述流程中的反应中,D到E为取代反应,E到F为还原反应
B.一定条件下I最多可以和9molH2反应
C.D的氢核磁共振谱图中有7组峰
D.G可以发生水解反应
(2)写出H的结构简式:___。
(3)写出F生成G的化学方程式:___。
(4)有机物X的分子组成比C发生消去反应后的产物多2个“CH2”,请写出X符合下列条件的同分异构体:___。
①X分子结构中不含碳碳双键和羟基②X核磁共振氢谱有三组峰
(5)以A和甲醇为原料合成B,请设计合成路线___(用流程图表示,无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)以石灰石为原料通过系列反应将硫元素以CaSO4的形式固定,从而降低SO2的排放。相关反应的热化学方程式如下:CaSO4 (s)+CO (g) ![]() CaO(s)+SO2 (g)+CO2 (g) △H1= +218.4kJ·mol-1(反应Ⅰ),CaSO4 (s) +4CO (g)
CaO(s)+SO2 (g)+CO2 (g) △H1= +218.4kJ·mol-1(反应Ⅰ),CaSO4 (s) +4CO (g) ![]() CaS(s) +4CO2(g)△H2=﹣175.6kJ·mol-1 (反应Ⅱ),结合反应Ⅰ、Ⅱ写出CaSO4 (s)与CaS (s) 反应的热化学反应方程式_______。
CaS(s) +4CO2(g)△H2=﹣175.6kJ·mol-1 (反应Ⅱ),结合反应Ⅰ、Ⅱ写出CaSO4 (s)与CaS (s) 反应的热化学反应方程式_______。
(2)NO2、SO2气体混合存在氧化物间的相互转化平衡:NO2(g)+SO2(g)![]() SO3(g)+NO(g),某活动小组对此反应进行研究实验
SO3(g)+NO(g),某活动小组对此反应进行研究实验
实验内容 | 实验现象 | 结论 | |
① | 将充有NO2、SO2气体的密闭烧瓶放入热水中 | 气体红棕色加深,一段时间后颜色不再变化 | △H___0 (填>、<或=) |
② | 在针筒中抽入5mL NO2和5mL SO2气体,封闭针筒前端,充分反应后,将活塞迅速推至5mL处 | 气体红棕色加深并保持不变 | 平衡____(填向左、向右或不)移动 |
③ | 在充有NO2、SO2混合气体的恒容容器中,达平衡后继续通入SO2气体 | _____ | 平衡向右移动,SO2的转化率____(填增大、减小或不变) |
(3)工业上用活性炭还原法处理NO,有关反应为:C(s) +2NO(g)![]() N2(g) +CO2(g)。为了提高NO的转化率,下列的措施可行的是___。
N2(g) +CO2(g)。为了提高NO的转化率,下列的措施可行的是___。
A.再加入一定量的碳 B.增大压强 C.用碱液吸收气体 D.使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:

①尿素水溶液热分解为NH3和CO2,该反应的化学方程式:___。
②反应器中NH3还原NO2的化学方程式:___。
③当燃油中含硫量较高时,尾气中SO2在O2作用下会形成(NH4)2SO4,使催化剂中毒。用化学方程式表示(NH4)2SO4的形成:__。
④尿素溶液浓度影响NO2的转化,测定溶液中尿素(M=60g·mol-1)含量的方法如下:取ag尿素溶液,将所含氮完全转化为NH3,所得NH3用过量的v1mLc1mol·L-1H2SO4溶液吸收完全,剩余H2SO4用v2mLc2mol·L-1NaOH溶液恰好中和,则尿素溶液中溶质的质量分数是__。
(2)NSR(NOx储存还原)工作原理:
NOx的储存和还原在不同时段交替进行,如图a所示。

①通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原。储存NOx的物质是__。
②用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,该过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应消耗的H2与Ba(NO3)2的物质的量之比是__。
③还原过程中,有时会产生笑气(N2O)。用同位素示踪法研究发现笑气的产生与NO有关。在有氧条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO。将该反应的化学方程式补充完整:___![]() □15NNO+□H2O___。
□15NNO+□H2O___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请结合题中数据,写出对应的热化学方程式。
(1)16gCH3OH(l)与适量O2反应,生成CO2(g)和H2O(l),放出683.4kJ热量_____。
(2)N2(g)和H2(g)反应生成2 molNH3(g),放出92.2kJ热量_____。
(3)稀溶液中,1molH2SO4与NaOH完全反应时,放出114.6kJ热量,写出表示中和热的热化学方程式_______。
(4)agC(s)与足量O2反应生成CO2气体时,放出bkJ热量____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中不是氧化还原反应的是
A. 3Cl2+6KOH===5KCl+KClO3+3H2O
B. CuO+H2![]() Cu+H2O
Cu+H2O
C. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
D. 2AgNO3+BaCl2===2AgCl↓+Ba(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】厌氧氨化法(Anammox)是一种新型的氨氮去除技术,原理如图所示。下列说法正确的是( )

A.1molNH4+所含的电子总数与1mol-OH所含的电子总数相同
B.过程II、III、IV均为还原反应
C.用该方法每处理1molNH4+需要的NO2-为0.5mol
D.1mol联氨(N2H4)中含有5mol共价键,均为σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】花青醛( )具有一种清新的花香,对香水和洗涤护理配方也非常有价值,下图是用Michael反应合成花青醛的一种合成路线。
)具有一种清新的花香,对香水和洗涤护理配方也非常有价值,下图是用Michael反应合成花青醛的一种合成路线。

已知:氨基连接在苯环上易被氧化。
回答下列问题:
(1)花青醛I中官能团的名称是___,可通过 直接判定___(选填编号)。
a.质谱 b.红外光谱 c.核磁共振氢谱
(2)A→B的反应方程式为___。
(3)B→C、C→D的反应类型分别是___、___。
(4)E的结构简式为____。
(5)对比分析说明,引入C→D与E→F步骤的目的是___。
(6)有机物G有多种同分异构体, 写出满足下列条件的一种同分异构体___。
①苯环上有3个取代基;②核磁共振氢谱有4个峰
(7)利用Michael反应, 以丙烯和 为原料合成
为原料合成 , 写出合成路线(无机试剂任选) ___。
, 写出合成路线(无机试剂任选) ___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com