
【题目】下图为阿托酸甲酯的一种合成路线:
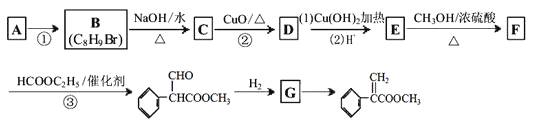
已知:反应③为取代反应,另一反应产物为乙醇
请回答下列问题:
(1)已知A为芳香烃,其核磁共振氢谱中出现5个蜂,其面积比为1:1:2:2:2,则A的名称为___________,若要检验有机物B的官能团,则所使用的试剂除了有机物B和水之外,还需要的试剂有________、________、________(填化学式)。
(2)写出有关的化学方程式
反应②____________________;
反应③____________________。
(3)阿托酸甲酯所含官能团的名称为____________________;阿托酸甲酯有多种同分异构体,其中苯环上只有一个支链,既能与NaHCO3溶液反应,又能使溴的四氯化碳溶液褪色的同分异构体有__________种(不考虑立体异构)。
(4)阿托酸甲酯的另外一种合成路线如下图所示:
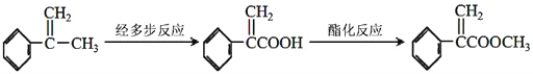
已知在多步反应过程中进行了下列4种不同的反应类型,请按照实际进行的反应顺序依次写出这四种反应类型的字母序号__________。
a.取代反应 b.消去反应 c.加成反应 d.氧化反应
【答案】苯乙烯NaOH溶液稀HNO3AgNO3溶液![]()
![]() 碳碳双键、酯基8cadb
碳碳双键、酯基8cadb
【解析】A为芳香烃,结合B的分子式可知,A为苯乙烯或乙苯、二甲苯,A的核磁共振氢谱中出现5个峰,其面积比为1:1:2:2:2,则A为![]() ,与溴化氢发生加成反应生成B,B发生卤代烃的水解反应生成C,C可以连续发生氧化反应,则B为
,与溴化氢发生加成反应生成B,B发生卤代烃的水解反应生成C,C可以连续发生氧化反应,则B为![]() ,C为
,C为![]() ,D为
,D为![]() ,E为
,E为![]() .苯乙酸与乙醇发生取代反应生成F为
.苯乙酸与乙醇发生取代反应生成F为![]() ,F与甲酸甲酯发生取代反应生成
,F与甲酸甲酯发生取代反应生成![]() ,
,![]() 与氢气发生加成反应生成G为
与氢气发生加成反应生成G为![]() ,G再发生消去反应得阿托酸乙酯;
,G再发生消去反应得阿托酸乙酯;
(1)由上述分析可知,A为![]() ,名称为苯乙烯,B为
,名称为苯乙烯,B为![]() ,含有的官能团为溴原子,检验溴原子方法为:将卤代烃在NaOH水溶液、加热条件水解得到NaBr,再用稀硝酸酸化,最后加入硝酸银溶液,有淡黄色沉淀生成;
,含有的官能团为溴原子,检验溴原子方法为:将卤代烃在NaOH水溶液、加热条件水解得到NaBr,再用稀硝酸酸化,最后加入硝酸银溶液,有淡黄色沉淀生成;
(2)反应②的化学方程式为:![]() ;反应③的化学方程式为:
;反应③的化学方程式为:![]() ;
;
(3)由阿托酸甲酯的结构可知,所含官能团有:酯基、碳碳双键;阿托酸甲酯有多种同分异构体,其中苯环上只有一个支链,能与NaHCO3溶液反应,含有-COOH,又能使溴的四氯化碳溶液褪色,含有碳碳双键,可以苯环取代烯酸烃基中H原子得到,烯酸有:CH2=CHCH2COOH,CH3CH=CHCOOH,CH2=C(CH3)COOH,烃基分别有3、3、2种H原子,故符合条件的同分异构体共有8种;
(4)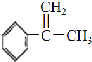 与溴发生加成反应得到
与溴发生加成反应得到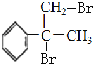 ,在在氢氧化钠水溶液、加热条件下发生水解反应得到
,在在氢氧化钠水溶液、加热条件下发生水解反应得到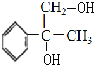 ,再发生氧化反应得到
,再发生氧化反应得到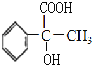 ,最后发生消去反应得到
,最后发生消去反应得到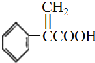 ,故答案为cadb。
,故答案为cadb。


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,W的单质是空气中体 积分数最大的气体,W与Y最外层电子数之和为X最外层电子数的2倍,X、Y、Z简单离子的电子层结构相同,Z最外层电子数等于最内层电子数。下列说法正确的是
A. 单质Z可用海水作原料获得
B. W的简单气态氢化物比Y的简单气态氢化物稳定
C. 原子半径由大到小的顺序:Z、Y、X、W
D. WX与ZX中的化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把元素周期表中第16号元素和第6号元素的原子相比较,下列数据中前者是后者的4倍的是( )
A.电子数
B.最外层电子数
C.中子数
D.次外层电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粗碘中通常含ICl和IBr,称为卤素互化物,其性质和卤素单质相似,都是较强的氧化剂,而且受热时ICl和IBr皆可像I2一样升华,在粗碘中加入以下选项中的一种物质后,再进行升华可制得精碘,应加入的物质是( )。
A. H2O B. Zn C. KI D. KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中能表示阿伏加德罗常数数值的是
A.1mol H+ 含有的电子数 B.标准状况下,22.4L酒精所含的分子数
C.1.6 g CH4 含有的质子数 D.1L 1mol/L的硫酸钠溶液所含的Na+ 数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是部分城市某日空气质量日报:
城市 | 污染指数 | 首要污染物 | 空气质量等级 | ||
SO2 | NO2 | PM10 | |||
A | 98 | 23 | 67 | SO2 | Ⅱ |
B | 47 | 29 | 35 | SO2 | Ⅰ |
C | 62 | 80 | 113 | PM10 | Ⅲ |
D | 52 | 76 | 59 | NO2 | Ⅰ |
(1) 由上表可知,空气质量日报中涉及的污染物主要是____________和可吸入颗粒物(PM10)。
(2) 汽车尾气则是城市大气中氮氧化物的主要来源之一。治理方法之一是在汽车排气管上加装“催化转化器”,使CO与NOx反应生成可参与大气生态环境循环的无毒气体,写出反应方程式_______________________________________。
(3) SO2的排放是造成酸雨的主要因素。形成酸雨的原理之一可简单表示如下:
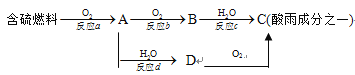
请回答下列问题:
①酸雨的pH____________(填“>”、“<”或“=”)5.6 ;
②反应b的化学方程式为____________________________________;
③在一段时间内连续不断测定溶液D的pH值,发现pH值变小,表示该变化的化学方程式是_________________。
④若用足量的氢氧化钠溶液吸收含二氧化硫的工业废气,写出该反应的离子方程式______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是
A. ![]() 的溶液中:Na+、K+、SiO32—、SO32-
的溶液中:Na+、K+、SiO32—、SO32-
B. pH=1的溶液中:K+、Al3+、SO42-、F—
C. 与镁反应生成氢气的溶液中:Na+、Ba2+、NO3-、Cl-
D. 0.1mol/L的NaHCO3溶液中:NH4+、Mg2+、Br-、AlO2-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.自发进行的反应一定是放热反应 B.非自发进行的反应一定是吸热反应
C.自发进行的反应一定能发生 D.有些吸热反应也能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一容积可变的容器中,反应2A(g)+B(g)![]() 2C(g)达到平衡时,A、B和C的物质的质量的量分别为4mol、2mol和4mol,保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
2C(g)达到平衡时,A、B和C的物质的质量的量分别为4mol、2mol和4mol,保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是( )
A. 均减半 B. 均加倍 C. 均减少1mol D. 均增加1mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com