
【题目】德国化学家凯库勒认为苯分子的结构中,碳碳间以单、双键交替结合而成环状。为了评价凯库勒的观点,某学生设计了以下实验方案:
实验操作:
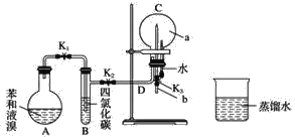
①按如图所示的装置图连接好各仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开K1、K2止水夹,关闭K3止水夹;
④待烧瓶C中气体收集满后,将导管b的下端插入烧杯里的水中,关闭K2,打开K3,挤压预先装有水的胶头滴管的胶头,观察实验现象。
请回答下列问题:
(1)能证明凯库勒观点错误的实验现象是_________。
(2)A中所发生的反应的反应类型为__________。
(3)A中发生反应的化学方程式__________。
(4)装置B的作用是____________。
【答案】C中产生“喷泉”现象 取代反应 ![]() +Br2
+Br2![]()
![]() +HBr 除去未反应的苯蒸气和溴蒸气
+HBr 除去未反应的苯蒸气和溴蒸气
【解析】
(1)依据凯库勒观点,苯环中含有双键,与溴发生加成反应,不会产生溴化氢,不会发生喷泉实验;
(2)(3)苯与溴在铁作催化剂的条件下发生取代反应生成溴苯和溴化氢;
(4)苯与液溴的反应是放热反应,苯与液溴均易挥发,溴的存在干扰检验H+、Br-,苯、溴容易溶于四氯化碳,四氯化碳是常用的有机溶剂。
(1)苯与溴如果发生加成反应,不产生溴化氢,无HBr在水中溶解导致的压强差,就不会发生喷泉实验;如果发生取代反应,则生成溴化氢,溴化氢易溶于水,能够发生喷泉实验,所以只要发生喷泉实验,就可证明苯与溴发生的是取代而不是加成反应,证明不含双键,可以证明凯库勒观点错误;
(2)苯与溴在铁作催化剂的条件下发生取代反应产生溴苯和HBr;
(3)在烧瓶A中发生的化学方程式为:![]() +Br2
+Br2![]()
![]() +HBr;
+HBr;
(4)由于反应放热,且苯与液溴均易挥发,苯和溴极易溶于四氯化碳,用四氯化碳除去溴化氢气体中的溴蒸气和苯,以防止干扰检验H+、Br-。


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】我国科学家设计了一种智能双模式海水电池,满足水下航行器对高功率和长续航的需求。负极为Zn,正极放电原理如图。下列说法错误的是( )
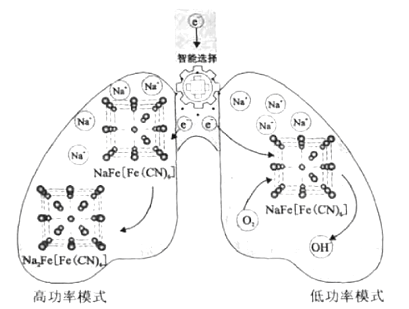
A. 电池以低功率模式工作时,NaFe[Fe(CN)6]作催化剂
B. 电池以低功率模式工作时,Na+的嵌入与脱嵌同时进行
C. 电池以高功率模式工作时,正极反应式为:NaFe[Fe(CN)6]+e-+Na+=Na2Fe[Fe(CN)6]
D. 若在无溶解氧的海水中,该电池仍能实现长续航的需求
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关如图所示原电池的说法正确的是
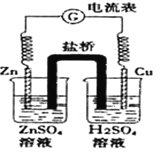
A. 随着反应进行,左烧杯中盐溶液浓度上升,右烧杯中酸溶液浓度下降
B. 盐桥的作用是让电子通过,以构成闭合回路
C. 随着反应进行,右烧杯中溶液pH变小
D. 总反应为:2H++ Zn ="==" H2↑+ Zn2+△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香叶醇是合成玫瑰香油的主要原料,其结构简式如下:
![]()
下列有关香叶醇的叙述正确的是( )
A.香叶醇的分子式为C10H18O
B.不能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
D.能燃烧,其产物一定为二氧化碳和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.向NaAlO2溶液中通入过量CO2:![]()
B.铝与氯化铜溶液反应:![]()
C.次氯酸钙溶液中通入SO2气体:![]()
D.在溶液中NH4HCO3与NaOH以等物质的量混合:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁过程中发生的主要反应为:![]() ,已知该反应在不同温度下的平衡常数如下:
,已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
请回答下列问题:
(1)该反应的平衡常数表达式![]() ______,该反应的正反应是______反应(填“放热”、“吸热”)。
______,该反应的正反应是______反应(填“放热”、“吸热”)。
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10 min后达到平衡。求该时间范围内反应的平均反应速率![]() ______、CO的平衡转化率
______、CO的平衡转化率![]() ______;
______;
(3)欲提高(2)中CO的平衡转化率,可采取的措施是______。
a.减少Fe的量 b.增加Fe2O3的量 c.移出部分CO2 d.提高反应温度e.减小容器的容积 f.加入合适的催化剂
(4)在氯氧化法处理含![]() 的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
①某厂废水中含KCN,其浓度为650mg/L。现用氯氧化法处理,发生如下反应(其中N均为![]() 价):
价):![]() 被氧化的元素是______。
被氧化的元素是______。
②投入过量液氯,可将氰酸盐进一步氧化为氮气。请配平下列化学方程式,并标出电子转移方向和数目:
□![]() □
□![]() □
□![]() □
□![]() □
□![]() □
□![]() □
□![]() ______
______
③若处理上述废水40L,使KCN完全转化为无毒物质,至少需液氯______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L密闭容器中投入一定量的A、B发生反应:3A(g)+bB(g)![]() cC(g) △H= -Q kJmol-1(Q>0),12s 时达到平衡,生成C的物质的量为0.8mol,反应过程如图所示。试计算:
cC(g) △H= -Q kJmol-1(Q>0),12s 时达到平衡,生成C的物质的量为0.8mol,反应过程如图所示。试计算:
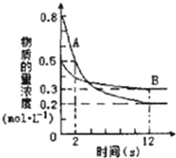
(1)前12s内,A的平均反应速率为______________。
(2)化学计量数之比b:c=______________。
(3)12s内,A和B反应放出的热量为__________(用Q表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述不正确的是( )
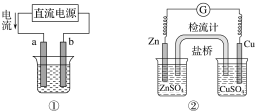
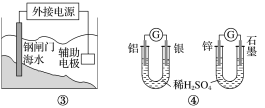
A.用图①装置实现铁上镀铜,a极为铜,电解质溶液可以是CuSO4溶液
B.图②装置盐桥中KCl的Cl-移向右烧杯
C.图③装置中钢闸门应与外接电源的负极相连获得保护
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通过反应:Al2O3+3C+3Cl2 ![]() 2AlCl3+3CO 制取无水氯化铝,下列关于该反应的说法正确的是
2AlCl3+3CO 制取无水氯化铝,下列关于该反应的说法正确的是
A.Al2O3是氧化剂B.CO是氧化产物
C.每生成1 mol AlCl3,转移3个电子D.C发生还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com