
����Ŀ����֪�������������ϳɰ���ӦΪ��N2��g��+3H2��g���T2NH3��g����H=��92kJmol��1��ش��������⣺
��1��ȡ1mol N2��g����3molH2��g������һ�ܱ������У�һ�������½��з�Ӧ����ƽ��ʱ����÷�Ӧ�ų�������92kJ������ڡ��������ڡ���С�ڡ�����ԭ�������������¶ȣ�������Ӧ�С�H����������С�����䡱����
��2����֪���ֱ��ƻ�1molN��H����1mol H��H����Ҫ���յ�����Ϊ��391kJ��436kJ�����ƻ�1mol N��N����Ҫ���յ�����Ϊ ��
��3��һ�������£������Ϊ2L�ĺ����ܱ������г���1molNH3��g�� ������������Ӧ������Ӻ�Ӧ�ﵽƽ�⣬���v��NH3��=0.40mol/��Lmin�����������ϳɰ���Ӧ��ƽ�ⳣ��Ϊ ��
��4�������������Ϊ1L�ĺ����ܱ������зֱ����1molN2��3molH2 �� ���ֱ�ֻ�ı�����һ���������ʱʹ��Ӧ�ﵽƽ�⣬��ð������������ʱ��ı仯��ͼ��ʾ�� 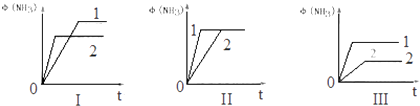
����ͼ���У�ֻ�ı��¶ȵ�Ϊ���I����II����III������ͬ����ֻ�ı�ѹǿ��Ϊ �� ֻ�ı������Ϊ ��
��5�����ѱ�״����8.96L����ͨ�뵽100g9.8%��������Һ�в���ȫ���գ�������Һ������Ũ�ȴӴ�С��˳���� ��
��6�������£���Ũ�Ⱦ�Ϊ0.1mol/L��MgCl2��FeCl3��AlCl3�����Һ��ͨ��NH3���������������ɳ����Ļ�ѧʽΪ �� ��pH=ʱ����ʼ����Mg��OH��2������ ����֪��Ksp[Mg��OH��2]=1.0��10��13�� Ksp[Fe��OH��3]=1.0��10��40��Ksp[Al��OH��3]=1.0��10��33��
���𰸡�
��1��С�ڣ������ǿ��淴Ӧ��1mol N2 ��3mol H2 �����ܱ������в�������ȫת��Ϊ2mol�İ��������Էų�����һ��С��92.0 kJ������
��2��946 kJ/mol
��3��![]()
��4����
��5��c��NH+����c��SO42������c��OH������c��H+��
��6��Fe��OH��3��6
���������⣺��1��N2 ��H2��Ӧ����2mol NH3ʱ�ų�������Ϊ92.0kJ����ָ1mol������1mol��������ȫ��Ӧ����2mol�İ����ų�������Ϊ92.0kJ��1mol N2 ��3mol H2 �����ܱ������в�������ȫת��Ϊ���������Էų�����һ��С��92.0 kJ����Ӧ�ȡ�H�����ʵĻ�ѧ�������йأ����ʵĻ�ѧ���������䣬�Ȼ�ѧ����ʽ�з�Ӧ�Ȳ��䣬���Դ��ǣ�С�ڣ������ǿ��淴Ӧ��1mol N2 ��3mol H2 �����ܱ������в�������ȫת��Ϊ2mol�İ��������Էų�����һ��С��92.0 kJ�����䣻��2����N��N�ļ���Ϊx��
���ڷ�ӦN2��g��+3H2��g��=2NH3��g����H=��92.0kJ/mol��
��Ӧ��=��Ӧ����ܼ��ܩ���������ܼ��ܣ���x+3��436kJ/mol��2��3��391kJ/mol=��92.0kJ/mol
��ã�x=946 kJ/mol��
���Դ��ǣ�946 kJ/mol��
����3��ƽ��ʱ��
2NH3��g�� | N2��g��+ | 3H2��g�� | ||
��ʼ��mol/L�� | 0.5 | 0 | 0 | |
ת����mol/L�� | 0.5��0.40 | 0.1 | 0.3 | |
ƽ�⣨mol/L�� | 0.3 | 0.1 | 0.3 |
K= ![]() =
= ![]() ��
��
�������ϳɰ���Ӧ��ƽ�ⳣ��K= ![]() =
= ![]()
���Դ��ǣ� ![]() ��4��ͼ����Ǹı��¶ȣ����·�Ӧ���ʼӿ죬�ﵽƽ��ʱ��̣���Ӧ���ȣ�ƽ�������ƶ�����T2��T1��
��4��ͼ����Ǹı��¶ȣ����·�Ӧ���ʼӿ죬�ﵽƽ��ʱ��̣���Ӧ���ȣ�ƽ�������ƶ�����T2��T1��
ͼ����ǼӴ���������ֻ�ı䷴Ӧ���ʣ�ƽ��״̬���ı䣻
ͼ���ı�ѹǿ������ѹǿ��Ӧ���ʼӿ죬ƽ�������ƶ�����P1��P2 ��
���Դ��ǣ���5����״����8.96L������0.4mol����ͨ�뵽100g9.8%��������Һ��0.1mol��������Һ�У�����0.1mol��NH4��2SO4 �� ����0.2molNH3H2O������c��NH+�����c��H+����С��������Һ������Ũ�ȴӴ�С��˳����c��NH+����c��SO42������c��OH������c��H+����
���Դ��ǣ�c��NH+����c��SO42������c��OH������c��H+������6������Al��OH��3��Mg��OH��2��Fe��OH��3���ܶȻ���������25���£���Ũ�Ⱦ�Ϊ0.1molL��1��AlCl3��MgCl2��FeCl3�����Һ��ͨ��NH3���������������ӿ�ʼ����ʱ��OH��Ũ�ȷֱ��ǣ� ![]() =1.0��10��13��
=1.0��10��13�� ![]() =2.15��10��11��
=2.15��10��11�� ![]() =1.0��10��6 �� ������ͬ��Ũ�ȵİ�ˮ��Fe��OH��3����������pH=��lg��1.0��10��6��=6���ʵ�pH=6ʱ����ʼ����Mg��OH��2������
=1.0��10��6 �� ������ͬ��Ũ�ȵİ�ˮ��Fe��OH��3����������pH=��lg��1.0��10��6��=6���ʵ�pH=6ʱ����ʼ����Mg��OH��2������
���Դ��ǣ�Fe��OH��3��6��
�����㾫����������Ĺؼ��������ⷴӦ�Ⱥ��ʱ�����֪ʶ�������ڻ�ѧ��Ӧ�зų������յ�������ͨ���з�Ӧ�ȣ��Լ��Ի�ѧƽ��ļ�������⣬�˽ⷴӦ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��


 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д� Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������CO2����ͨ��NaOH��Ca��OH��2��NaAlO2�Ļ����Һ�С���֪NaAlO2��CO2��Ӧ����Al��OH��3���������ɳ��������ʵ�����ͨ��CO2������Ĺ�ϵ�ɱ�ʾΪ��������
A. 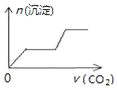 B.
B. 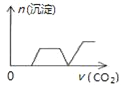
C.  D.
D. 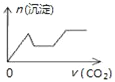
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ú�ң���Ҫ����SiO2��Fe2O3��Al2O3�ȣ���ȼú��������в����ķ�������ú�ҵ��ۺ����þ��кܴ�ļ�ֵ��
���о���Աͨ��ʵ��Է�ú����������Ԫ�صķ��빤�ս������о���
��1����������Һ�ֽ��ú�ң�ʹ���е�������Ԫ���ܳ�������ʵ�ֳ������룮
��д��������Һ��Fe2O3��Ӧ�����ӷ���ʽ ��
�ڳ�������õ���������Ҫ�ɷ��� ��
��2����1���������õ���Һ�м��뻹ԭ��ʹFe3+ת��ΪFe2+ �� ��ϱ�������ԭ�� ��
���� | Fe��OH��2 | Fe��OH��3 | Al��OH��3 |
�������䣨pH�� | 7.06��8.95 | 1.94��3.20 | 3.69��4.8 |
��3��ʹ�ü��Խ����İ�ˮΪpH���ڼ������з���ʵ�飮
�ٰ�ˮʹ��Һ�������ӳ��������ӷ���ʽΪ ��
�ڷ�Ӧ�յ��pH������������Ч����Ӱ����ͼ1������ʵ������Ϊ�ﵽ�õķ���Ч������Ӧ�����п���pH�ķ�Χ�� �� ѡ��÷�Χ�������� �� 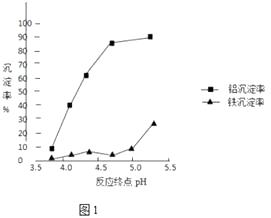
��4����NH4HSO4��H2SO4�����ʵ�����1��1������Ƴɽ�ȡҺ��220��ʱ���ɽ�������ú����Al2O3ת��Ϊ�������[NH4Al��SO4��2]��Ȼ����롢���ջ�ô�Al2O3 ��
��֪������泥����ܽ�ȣ�0��ʱ��S=5.2g��100��ʱ��S=421.9g��
��280��ʱ�ֽ⣮
�������Ͽ�֪��������������������ʷ���ķ����� ��
��5������NH4Al��SO4��2ͬʱ�õ�������壨NH3��N2��SO2��SO3��H2O������16mol������尴ͼ2װ�ñ���ȫ�����Ƶý�ȡҺ���뽫ͼ2���Լ��������ʵ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ������Ũ�Ⱦ�Ϊ0.1mol/L��������Һ������Ũ�ȹ�ϵ��ȷ������֪��H2C2O4���ڶ�Ԫ���ᣮ�� ��
A.Na2S��Һ��c��Na+����c��S2������c��HS������c��OH������c��H2S��
B.Na2CO3��Һ��c��Na+��+c��H+��=c��CO ![]() ��+c��HCO
��+c��HCO ![]() ��+c��OH����
��+c��OH����
C.Na2C2O4��Һ��c��OH����=c��H+��+c��HC2O ![]() ��+2c��H2C2O4��
��+2c��H2C2O4��
D.CH3COONa��CaCl2�����Һ��c��Na+��+c��Ca2+��=c��CH3COO����+c��CH3COOH��+2c��Cl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ���������ֵ,����˵����ȷ���ǣ� ��
A. 120��NaHSO4���庬��������ĿΪ3NA
B. ������Ϊ1g��O2��N2������庬�еĵ�����Ϊ0.5NA
C. Na2O2��CO2��Ӧʱ��ÿ����1 mol O2ת�Ƶ�����ΪNA
D. ����FeI2����Һ��ͨ������Cl2������1 mol Fe2+������ʱ����ת�Ƶ�����ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʷ�����ȷ���ǣ� ����
A. SO2��SiO2��CO��CO2��Ϊ���������ҲΪ�ǽ���������
B. �ɱ�����������ˮ������Ϊ�����ҲΪ������
C. ϡ����������������Һ���Ȼ�����Һ��Ϊ���壬ҲΪ�����
D. ����������������������(CuSO4��5H2O)�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��KMnO4��һ�ֵ��͵�ǿ�����������������գ�
������KMnO4������Һ����Cu2S��CuS�Ļ����ʱ�������ķ�Ӧ���£�
�� MnO4��+ Cu2S + H+�� Cu2+ + SO2�� + Mn2+ + H2O (δ��ƽ)
�� MnO4��+ CuS + H+ �� Cu2+ + SO2�� + Mn2+�� H2O (δ��ƽ)
��1�����й��ڷ�Ӧ�ٵ�˵���д������_________��ѡ���ţ���
a����������Ԫ����Cu��S b���������뻹ԭ�������ʵ���֮��Ϊ8:5
c����ԭ�Ե�ǿ����ϵ�ǣ� Mn2+<Cu2S d��ÿ����2.24 L(���) SO2��ת��0.6mol����
��2����ƽ�������Ӧ���е���ת�Ƶķ������Ŀ��_____
MnO4��+ CuS + H+ �� Cu2+ + SO2�� + Mn2+�� H2O
��3������H2O2����KMnO4�з�Ӧ��2KMnO4+7H2O2+3H2SO4= K2SO4+2MnSO4+6O2��+10H2O����1molKMnO4������H2O2��_________mol��
II����֪�ڼ��������£�MnO4����e������MnO42�� (��ɫ)
��4�� ��KMnO4��Һ����NaOH��Һ���ȣ��õ�������ɫ��Һ���������������ɣ�д����Ӧ�����ӷ���ʽ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2�������Ϊ��Ҫԭ����ȡ1��2��������ʱ����Ҫ�����ķ�Ӧ�����ǣ� ��
A.�ӳɡ���ȥ��ȡ��
B.��ȥ���ӳɡ�ȡ��
C.ȡ������ȥ���ӳ�
D.ȡ�����ӳɡ���ȥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˲ⶨ��ҵ������Na2CO3������������������NaCl�����ס�����λѧ���ֱ������һ������ѧ����ʵ��������ͼ��ʾ��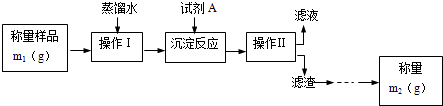
ѧ������Ƶ�ʵ�鲽�����£�
�ٳ�ȡ��Ʒ��Ϊ1.150g��
���ܽ�����250mL��Һ��
��ȡ20mL������Һ��������� 2��3�Σ�
����0.1140mol/L�ı�������еζ���
�����ݴ�����
�ش��������⣺
��1����ѧ����Ƶķ������Լ�A����ѡ�������ţ�
a��CaCl2 b��BaCl2 c��AgNO3
��2���������Ӧ���������ν��Т�������ʵ��������裮���У�֤��ǰ��һ���IJ����Ѿ���ɵķ�������
��3��ѧ����ij��ʵ�鿪ʼ�ζ�ʱ��������Һ�Ŀ̶���0.00mL����������ʱ�ﵽ�ζ��յ㣬��ʱ������Һ�Ŀ̶���14.90mL������ͬѧ�Ըô�ʵ�����ݼ������Ʒ��Na2CO3��������������������λС��������ͬѧ�����ʵ��������ʦ����������ֵ�dz��ӽ�������ʦ�����϶�����ʵ�鷽����Ʋ��ϸ�����Ϊ���ܵ�ԭ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com