
 数与中子数相等,能与B形成DB2、DB3常见化合物。根据以上条件,回答下列问题:
数与中子数相等,能与B形成DB2、DB3常见化合物。根据以上条件,回答下列问题:科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碱金属的单质中,锂的还原性最强 |
| B.第ⅠA族元素比第ⅡA族元素的金属性强 |
| C.随着核电荷数的递增,卤族元素的气态氢化物的稳定性逐渐减弱 |
| D.随着核电荷数的递增,第三周期元素的氧化物对应的水化物的酸性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 ;由R生成Q的化学方程式: 。
;由R生成Q的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
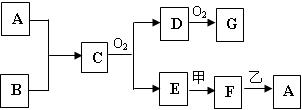
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
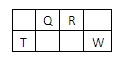
| A.Q形成的化合物的种类最多 |
| B.T位于元素周期表的第三周期第III族 |
| C.Q和R的气态氢化物,前者比后者稳定 |
| D.原子及简单离子半径均是T>W |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | | | ② | ④ | |
| 3 | ⑤ | | ③ | | ⑧ | ⑥ | ⑦ | |
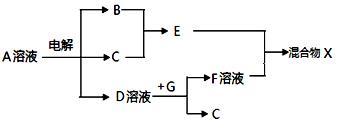
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硼元素(相对原子质量为10.8)只有两种同位素10B与11B,则其原子质量比为1:4 |
| B.共价化合物中可能有离子键,离子化合物中可能有共价键 |
| C.和原子序数为x的第ⅡA族元素同周期的第ⅢA族元素的原子序数可能是x+1或x+11或x+25 |
| D.原子序数小于11的两种元素原子的核外电子层数之比与最外层电子数之比相等的元素共有3对 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com