
| A、负极反应式:Ag+Cl-+e-═AgCl |
| B、电池的正极用二氧化锰纳米棒为材料,可大大提高发电效率 |
| C、Na+不断向“水”电池的负极移动 |
| D、每转移2 mol电子,正极就有5 mol MnO2被氧化 |


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定温度下的可逆反应,只有达到平衡时才具有平衡常数 |
| B、化学平衡移动时,平衡常数一定改变 |
| C、化学平衡常数大的可逆反应,所有反应物的转化率一定大 |
| D、对于一个确定的反应来说,平衡常数的数值越大,反应限度越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由C(石墨,s)═C(金刚石,s)△H=+1.9 kJ?mol-1可知,石墨比金刚石稳定性差 |
| C、CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+566.0kJ/mol |
| D、在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、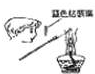 检验溶液中K离子是否存在 |
B、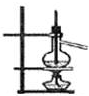 分离沸点相差较大的溶液体混合物 |
C、 向容量瓶中转移液体 |
D、 分离互不相溶的两种液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
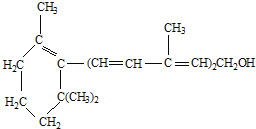
| A、②④ | B、①③ |
| C、③④ | D、全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用天平称取6.72g硫酸铜,加入500mL水 |
| B、用天平称取7.0g硫酸铜,加入500mL水 |
| C、用天平称取12.5g胆矾,配成500mL溶液 |
| D、用天平称取10.5g胆矾,配成500mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
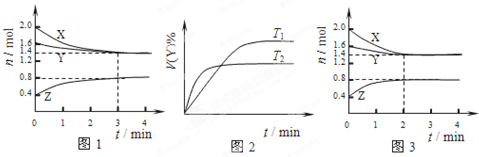
| A、容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g) |
| B、反应进行前3min内,用X表示的反应速率v(X)=0.1mol/(L?min) |
| C、若改变反应条件,使反应进程如图3所示,则改变的条件是使用催化剂 |
| D、保持其他条件不变,升高温度,化学平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、新制氯水保存在无色玻璃试剂瓶中 |
| B、氢氧化钠溶液保存在带橡皮塞的玻璃试剂瓶中 |
| C、少量的钠保存在煤油中 |
| D、二氧化硅常用于制造光导纤维 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com