
20ŹĄ¼Ķ70Äź“śŅŌĄ“£¬ČĖĆĒÖš½„ČĻŹ¶µ½£¬Čē¹ū¼ĢŠų¹ż¶ąµŲŅĄĄµŹÆÓĶ×÷ĪŖÖ÷ŅŖÄÜŌ“£¬³ŁŌē»į³öĻÖŃĻÖŲµÄÄÜŌ“Ī£»ś£¬½ńĢģµÄĻÖŹµ£¬²»Ö¹Ņ»“ĪµŲÖ¤Ć÷ĮĖÕāŅ»µć£”Ņņ“Ė£¬ĪŅĆĒ±ŲŠėŌŚ½ŚŌ¼Ź¹ÓƵÄĶ¬Ź±£¬Ń°ÕŅŠĀµÄĢę“śÄÜŌ“”£Ēė¼ņŅŖ»Ų“šĻĀĮŠÓŠ¹ŲµÄĪŹĢā£ŗ
£Ø1£©ŅŌŹÆÓĶĪŖĄż£¬ĒėÄć·ÖĪöŗĶ¹éÄÉ£¬×÷ĪŖŅ»ÖÖ±Č½ĻŗƵÄÄÜŌ“Ó¦øĆ¾ßÓŠÄÄŠ©ĢŲµć£æ
£Ø2£©Čē¹ūÓĆĆŗ”¢ĢģČ»Ęų”¢ĒāÄÜ”¢ÉśĪļÖŹÄÜ”¢ŗĖÄÜ”¢·ēÄܵȥ“Ģę“śŹÆÓĶ×÷ĪŖÖ÷ŅŖÄÜŌ“£¬ÕāŃł×öæÉÄÜĆęĮŁ»ņæÉÄÜ“ųĄ“µÄÖ÷ŅŖĪŹĢā·Ö±šŹĒŹ²Ć“£æÄćČĻĪŖÓ¦øĆŌõŃł×ö»įøüŗĆŠ©£æ
£Ø3£©Ćŗ”¢ŹÆÓĶŗĶĢģČ»ĘųµČ»ÆŹÆČ¼ĮĻŹĒÓ¦øĆ×÷ĪŖÄÜŌ“Ź¹ÓĆ£¬»¹ŹĒÓ¦øĆ×÷ĪŖŌĮĻ¼Ó¹¤³ÉŅ½Ņ©”¢»Æ¹¤²śĘ·£æ¶ŌÕāŃłÓŠÕłŅéµÄĪŹĢā£¬ÄćµÄæ“·ØŹĒŹ²Ć“£æĒėøł¾ŻÄćÕĘĪÕµÄÓŠ¹ŲŹż¾ŻŗĶ׏ĮĻĖµĆ÷ÄćµÄ¹Ūµć”£
 ½ņĒŽĢÓż¼ĘĖ抔דŌŖĻµĮŠ“š°ø
½ņĒŽĢÓż¼ĘĖ抔דŌŖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2012-2013Ń§ÄźÉ½¶«Ź”¼ĆÄžŹŠćōĖ®Ņ»ÖŠø߶ž12ŌĀÖŹĮæ¼ģ²ā»ÆѧŹŌ¾ķ£Ø“ų½āĪö£© ĢāŠĶ£ŗĢīæÕĢā
£Ø6·Ö£©øßĢśĖį¼ŲŹĒ20ŹĄ¼Ķ70Äź“śŅŌĄ“æŖ·¢µÄŅ»ÖÖ¼Ģ³ōŃõ”¢¹żŃõ»ÆĒā”¢¶žŃõ»ÆĀČÖ®ŗóŅ»ÖÖŠĀŠĶĖ®“¦Ąķ¼Į,ĖüÄÜæģĖŁÉ±ĆšĖ®ÖŠµÄĻø¾śŗĶ²”¶¾,ĒŅ²»»įÉś³ÉČżĀČ¼×Ķ锢ĀČ“ś·ÓµČ“Ī¼¶ŃÜÉśĪļ”£øßĢśĖįøł£ØFeO42££©ŌŚČÜŅŗÖŠ³Ź×ĻŗģÉ«£¬ČÜŅŗµÄpH¶ŌøßĢśĖįøłĪČ¶ØŠŌµÄÓ°ĻģŗÜ“ó,µ±pHÖµĪŖ10-11Ź±·Ē³£ĪČ¶Ø£¬¶ųµ±pH<7.5Ź±,ĪČ¶ØŠŌĆ÷ĻŌĻĀ½µ,·Ö½ā·Å³öŃõĘų,²¢Īö³ö¾ßÓŠø߶ČĪüø½»īŠŌµÄĪŽ»śŠõÄż¼ĮFe(OH)3”£µē½ā·ØÖʱøøßĢśĖį¼ŲŌĄķČēÓŅĶ¼ĖłŹ¾”£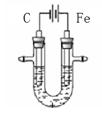
(1) µē½āÖŹČÜŅŗӦєÓĆ______________
A”¢NaOHČÜŅŗ B”¢NaClČÜŅŗ C”¢Ļ”ĮņĖį
(2) µē½ā¹ż³ĢÖŠæÉÄܹŪ²ģµ½µÄŹµŃéĻÖĻóÓŠ ”£
(3) Éś³ÉøßĢśĖįøł£ØFeO42££©µÄµē¼«·“Ó¦ŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2014½ģɽ¶«Ź”¼ĆÄžŹŠø߶ž12ŌĀÖŹĮæ¼ģ²ā»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£Ø6·Ö£©øßĢśĖį¼ŲŹĒ20ŹĄ¼Ķ70Äź“śŅŌĄ“æŖ·¢µÄŅ»ÖÖ¼Ģ³ōŃõ”¢¹żŃõ»ÆĒā”¢¶žŃõ»ÆĀČÖ®ŗóŅ»ÖÖŠĀŠĶĖ®“¦Ąķ¼Į,ĖüÄÜæģĖŁÉ±ĆšĖ®ÖŠµÄĻø¾śŗĶ²”¶¾,ĒŅ²»»įÉś³ÉČżĀČ¼×Ķ锢ĀČ“ś·ÓµČ“Ī¼¶ŃÜÉśĪļ”£øßĢśĖįøł£ØFeO42££©ŌŚČÜŅŗÖŠ³Ź×ĻŗģÉ«£¬ČÜŅŗµÄpH¶ŌøßĢśĖįøłĪČ¶ØŠŌµÄÓ°ĻģŗÜ“ó,µ±pHÖµĪŖ10-11Ź±·Ē³£ĪČ¶Ø£¬¶ųµ±pH<7.5Ź±,ĪČ¶ØŠŌĆ÷ĻŌĻĀ½µ,·Ö½ā·Å³öŃõĘų,²¢Īö³ö¾ßÓŠø߶ČĪüø½»īŠŌµÄĪŽ»śŠõÄż¼ĮFe(OH)3”£µē½ā·ØÖʱøøßĢśĖį¼ŲŌĄķČēÓŅĶ¼ĖłŹ¾”£

(1) µē½āÖŹČÜŅŗӦєÓĆ______________
A”¢NaOHČÜŅŗ B”¢NaClČÜŅŗ C”¢Ļ”ĮņĖį
(2) µē½ā¹ż³ĢÖŠæÉÄܹŪ²ģµ½µÄŹµŃéĻÖĻóÓŠ ”£
(3) Éś³ÉøßĢśĖįøł£ØFeO42££©µÄµē¼«·“Ó¦ŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
øßĢśĖį¼ŲŹĒ20ŹĄ¼Ķ70Äź“śŅŌĄ“æŖ·¢µÄŅ»ÖÖ¼Ģ³ōŃõ”¢¹żŃõ»ÆĒā”¢¶žŃõ»ÆĀČÖ®ŗóŅ»ÖÖŠĀŠĶĖ®“¦Ąķ¼Į,ĖüÄÜæģĖŁÉ±ĆšĖ®ÖŠµÄĻø¾śŗĶ²”¶¾,ĒŅ²»»įÉś³ÉČżĀČ¼×Ķ锢ĀČ“ś·ÓµČ“Ī¼¶ŃÜÉśĪļ”£øßĢśĖįøł£ØFeO42££©ŌŚČÜŅŗÖŠ³Ź×ĻŗģÉ«£¬ČÜŅŗµÄpH¶ŌøßĢśĖįøłĪČ¶ØŠŌµÄÓ°ĻģŗÜ“ó,µ±pHÖµĪŖ10-11Ź±·Ē³£ĪČ¶Ø£¬¶ųµ±pH<7.5Ź±,ĪČ¶ØŠŌĆ÷ĻŌĻĀ½µ,·Ö½ā·Å³öŃõĘų,²¢Īö³ö¾ßÓŠø߶ČĪüø½»īŠŌµÄĪŽ»śŠõÄż¼ĮFe(OH)3”£µē½ā·ØÖʱøøßĢśĖį¼ŲŌĄķČēÓŅĶ¼ĖłŹ¾”£
(1) µē½āÖŹČÜŅŗӦєÓĆ______________
A”¢NaOHČÜŅŗ”””” B”¢NaClČÜŅŗ”” C”¢Ļ”ĮņĖį
(2) µē½ā¹ż³ĢÖŠæÉÄܹŪ²ģµ½µÄŹµŃéĻÖĻóÓŠ”””””””””” ”£
(3) Éś³ÉøßĢśĖįøł£ØFeO42££©µÄµē¼«·“Ó¦ŹĒ”””””””””””” ”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
(1)øßĢśĖį¼ŲŹĒ20ŹĄ¼Ķ70Äź“śŅŌĄ“æŖ·¢µÄŅ»ÖÖ¼Ģ³ōŃõ”¢¹żŃõ»ÆĒā”¢¶žŃõ»ÆĀČÖ®ŗóŅ»ÖÖŠĀŠĶĖ®“¦Ąķ¼Į,ĖüÄÜæģĖŁÉ±ĆšĖ®ÖŠµÄĻø¾śŗĶ²”¶¾,ĒŅ²»»įÉś³ÉČżĀČ¼×Ķ锢ĀČ“ś·ÓµČ“Ī¼¶ŃÜÉśĪļ”£øßĢśĖįøł£ØFeO42££©ŌŚČÜŅŗÖŠ³Ź×ĻŗģÉ«£¬ČÜŅŗµÄpH¶ŌøßĢśĖįøłĪČ¶ØŠŌµÄÓ°ĻģŗÜ“ó,µ±pHÖµĪŖ10-11Ź±·Ē³£ĪČ¶Ø£¬¶ųµ±pH<7.5Ź±,ĪČ¶ØŠŌĆ÷ĻŌĻĀ½µ,·Ö½ā·Å³öŃõĘų,²¢Īö³ö¾ßÓŠø߶ČĪüø½»īŠŌµÄĪŽ»śŠõÄż¼ĮFe(OH)3”£µē½ā·ØÖʱøøßĢśĖį¼ŲŌĄķČēÓŅĶ¼ĖłŹ¾”£
µē½āÖŹČÜŅŗӦєÓĆ______________
A”¢NaOHČÜŅŗ”””” B”¢NaClČÜŅŗ”” C”¢Ļ”ĮņĖį
(2) µē½ā¹ż³ĢÖŠæÉÄܹŪ²ģµ½µÄŹµŃéĻÖĻóÓŠ”””””””””” ”£
(3) Éś³É øßĢśĖįøł£ØFeO42££©µÄµē¼«·“Ó¦ŹĒ”””””””””””” ”£
øßĢśĖįøł£ØFeO42££©µÄµē¼«·“Ó¦ŹĒ”””””””””””” ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com