
����Ŀ������ƽ�ⳣ���Ǻ���������ʵ���̶ȵ�����������֪��
��ѧʽ | ���볣��(25 ��) |
HCN | K��4.9��10��10 |
CH3COOH | K��1.8��10��5 |
H2CO3 | K1��4.3��10��7��K2��5.6��10��11 |
��1��25 ��ʱ���е�Ũ�ȵ�NaCN��Һ��Na2CO3��Һ��CH3COONa��Һ������Һ��pH�ɴ�С��˳��Ϊ________(�û�ѧʽ��ʾ)��
��2����NaCN��Һ��ͨ��������CO2��������Ӧ�Ļ�ѧ����ʽΪ_____________��
��3��25 ��ʱ����CH3COOH��CH3COONa�Ļ����Һ�У������pH��6������Һ��c(CH3COO��)��c(Na��)��________ mol��L��1(�ȷֵ)��c(CH3COO��)/c(CH3COOH)��________��
���𰸡�Na2CO3��NaCN��CH3COONa NaCN��H2O��CO2��HCN��NaHCO3 9.9��10��7 18
��������
��1����������ˮ��Ĺ��ɣ�Խ��Խˮ�⣬ˮ��̶�Խ����Һ��pHֵԽ���ݵ���ƽ�ⳣ�����ж����Ե�ǿ��˳��Ϊ��CH3COOH��HCN��HCO3-����pH�ɴ�С��˳��ΪNa2CO3��NaCN��CH3COONa��
��2���������Ե�ǿ��˳��Ϊ��CH3COOH��HCN��HCO3-�������ǿ���Ʊ������֪��NaCN��Һ��ͨ��������CO2��������Ӧ�Ļ�ѧ����ʽΪNaCN��H2O��CO2��HCN��NaHCO3��
��3�������£�Kw=10-14����pH��6����Һ�������Ӻ�������Ũ�ȷֱ���10-6mol/L��10-8mol/L��������Һ�ʵ����Կɵã�c(Na��)+c��H������c(CH3COO��)+c��OH-����c(CH3COO��)��c(Na��)��c��H����-c��OH-��=10-6 mol/L-10-8 mol/L =9.9��10��7mol/L��c(CH3COO��)/c(CH3COOH)��c(CH3COO��)��c��H����/[c(CH3COOH)��c��H����]=K/c��H����=![]() =18��
=18��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij�ϴ���(��ZnO��CuO��Fe2O3��ʯī��MnO2��)�л��ս�������ȡ��������п�Ĺ�����������(��֪��Zn������������������������Al������Ӧ��������������)��
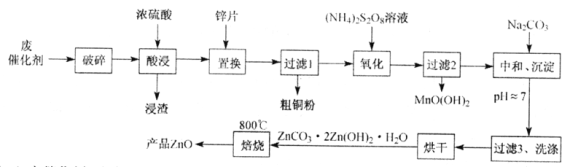
��1���ϴ�������������Ŀ����____________________________________________��
��2����������ʱMn2+�����������ӷ���ʽΪ_________________________________��
��3�����к͡�������ʱ����pH���ߣ����ʽ̼��п�IJ���ƫС��д���䷴Ӧ�����ӷ���ʽ(��дһ������)��____________________________________________��
��4���������ͭ������ͭ������������ʵ�鲽�����£�
I.ȷ��ȡ��ͭ��mg���������������H2O2��Һʹ����ȫ�ܽ⡣
��.����Һ���1~2min����ȥ������H2O2��
��.�������ڱμ��ų�Fe3+�ĸ��š�Ȼ������Թ�����KI��Һ(��Ӧ��2Cu2++4I��=2CuI��+I2)���ټ��뼸�ε�����Һ��ָʾ������ c mol ��L��1Na2S2O3����Һ�ζ�����ɫ��ʧ(I2+2S2O32��=2I��+S4O62��)�Ұ�����ڲ���ɫ��������Na2S2O3����ҺVmL��
��ͭ����������Ϊ______________________��
��ȱ�ٲ��������ʹ��õ�ͭ����������___________(����ƫ��������ƫС��������������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶���,���һ�����ܱ������н������¿��淴Ӧ:X(g)+Y(g)![]() Z(g)+W(s)����H>0������������ȷ����(����)
Z(g)+W(s)����H>0������������ȷ����(����)
A. ��������W,�淴Ӧ��������,����Ӧ���ʼ�С B. �����¶�,ƽ�������ƶ�
C. ������������ѹǿ����ʱ,��Ӧ�ﵽƽ�� D. ��Ӧƽ������X,������Ӧ�Ħ�H����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.20mol��L-1��NaOH��Һ�ζ�10.00mL 0.20mol��L-1��NaHSO3��Һ���ζ���������Һ��pH�仯�͵μ�NaOH��Һ�������ϵ��ͼ��ʾ������˵��������ǣ� ��

A.��Һ��ˮ�ĵ���̶ȣ�b>a>c
B.pH=7ʱ�����ĵ�V(NaOH)<10.00mL
C.��������K2(H2SO3)ԼΪ1.0��10��7
D.c����Һ��c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������廯̨���������������ڵ��ƾ��в�ݮ�����ѡ�ӣ�ҡ�����������ζ��ʳ���㾫�������ģ����ͼ��ʾ(ͼ��������֮��Ĺ�������ѧ�����絥����˫����)�����Ʊ������漰�����Ʊ����ȩ�����ȩ�����Ʊ�����ᣬ����״������Ƶá�����˵������ȷ����

A. ���������ķ���ʽΪC10H10O2
B. �������Ƶõ����ȩ�ڵ��ص���������
C. 1mol����������H2�ӳ��������4mol
D. ��������������̼ԭ�ӿ�����ͬһƽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1 mol H��H���ļ�����436kJ��1 mol I��I���ļ�����151kJ��1 mol H��I���ļ�����299kJ����Է�ӦH2��g��+I2��g��![]() 2HI��g����˵��������ȷ���� �� ��
2HI��g����˵��������ȷ���� �� ��
A.���ȷ�ӦB.���ȷ�ӦC.���Ϸ�ӦD.���淴Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H3BO3����ͨ�����NaB(OH)4��Һ�ķ����Ʊ����乤��ԭ����ͼ�����������������( )

A. M�ҷ����ĵ缫��ӦʽΪ��2H2O��4e�� = O������4H��
B. N����a% <b%
C. bĤΪ��Ĥ����Ʒ�ҷ�����Ӧ�Ļ�ѧԭ��Ϊǿ��������
D. ������ÿ����1mol��Ʒ�������ҿ����ɱ�״����5.6L����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ��(ƽ���ƶ�ԭ��)���͵���
����ˮ�д��ڻ�ѧƽ�⣺Br2��H2O ![]() HBr��HBrO��������AgNO3��Һ����Һ��ɫ��dz
HBr��HBrO��������AgNO3��Һ����Һ��ɫ��dz
�����ڳ�ʪ�Ŀ�����������
�۶���������������������ƽ����ϵ������ѹǿ����ɫ����
�ܺϳɰ���Ӧ��Ϊ��߰��IJ��ʣ�������Ӧ��ȡ�����¶ȵĴ�ʩ
�������Ȼ��ع����Ʊ��أ�Na(l)��KCl(l) ![]() K(g)��NaCl(l)
K(g)��NaCl(l)
A.�٢�B.�ۢ�C.�ڢ�D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Գ�����0.1mol/L�Ĵ�����Һ������˵����ȷ����
A.��ˮ���������c(H+)=1.0��10-13mol/L
B.c(CH3COOH)��c(H+)��c(CH3COO-)��c(OH-)
C.��ͬŨ�ȵ�����ֱ��ˮϡ��10����pH(����) <pH(����)
D.���Ũ�ȵ����NaOH��Һ��Ӧ�����Һ�У�c(CH3COOH)+c(CH3COO-)=0.1mol/L
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com