
| A. | 甲烷和氯气混合光照 | B. | 苯酚与溴水反应 | ||
| C. | 丙烯和氯化氢发生加成反应 | D. | 1-丁烯和氢气发生加成反应 |
分析 A.光照下甲烷取代反应为链锁式反应;
B.苯酚与溴水发生取代反应生成三溴苯酚和溴化氢;
C.丙烯结构不对称,与HCl可发生加成反应生成两种产物;
D.1-丁烯与氢气发生加成反应生成丁烷.
解答 解:A.光照下甲烷取代反应为链锁式反应,生成HCl及四种卤代烃,为混合物,故A错误;
B.苯酚与溴水反应生成三溴苯酚和HBr的混合物,故B错误;
C.丙烯结构不对称,与HCl可发生加成反应生成两种产物为2-氯-丙烷、1-氯-丙烷,为混合物,故C错误;
D.1-丁烯与氢气发生加成反应生成的产物只有丁烷,故D正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意常见有机物的性质及反应,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 营养强化剂--酱油中加铁、加锌 | B. | 调味剂--亚硝酸钠、味精 | ||
| C. | 防腐剂--氯化钠、柠檬黄 | D. | 着色剂--胡萝卜素、苯甲酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 配料表 | 精制海盐、碘酸钾[ |
| 含碘量 | 20~40mg/kg |
| 卫生许可证号 | ××卫碘字(1999)第001号 |
| 分装日期 | 见封底 |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时,待食品熟后加入碘盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ⑤ | C. | ④⑤ | D. | ② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X分子中最多可有9个碳原子共平面 | |
| B. | X可以发生取代、加成、聚合等反应 | |
| C. | 1 mol X与足量NaHCO3溶液反应所得物质的分子式为C9H7O4Na | |
| D. | 苯环上的取代基与X完全相同的X的同分异构体有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某离子第三层上和第二层上的电子数均为第一层的4倍 | |
| B. | Cl-的结构示意图: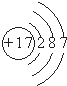 | |
| C. | 某物质的焰色反应为黄色,某物质一定为钠的化合物 | |
| D. | 14C和14N的质量数相等,互称为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=c(Cl-)+c(OH-) | |
| B. | 由水电离出的c(H+)=1.0×10ˉ 2 mol•Lˉ1 | |
| C. | 与等体积PH=12的氨水混合后所得溶液显中性 | |
| D. | 与等体积0.01 mol•Lˉ1CH3COONa溶液混合后所得溶液中:c(Cl-)=c(CH3COO-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com