
��֪������ʱ��ˮ�д��ڵ���ƽ�⣺![]() ������������ȷ����
������������ȷ����
![]() A�������¶ȣ�ˮ�ĵ���̶�����c(H+)����pH<7��������Һ������
A�������¶ȣ�ˮ�ĵ���̶�����c(H+)����pH<7��������Һ������
![]() B����ˮ�м��백ˮ��ƽ�����淴Ӧ�����ƶ���ˮ�ĵ����ܵ����ƣ�����c(OHһ)����
B����ˮ�м��백ˮ��ƽ�����淴Ӧ�����ƶ���ˮ�ĵ����ܵ����ƣ�����c(OHһ)����
![]() C����ˮ�м����������ᣬc(H��)����������ˮ�������c(H+)>1��10-7mol��L
C����ˮ�м����������ᣬc(H��)����������ˮ�������c(H+)>1��10-7mol��L
![]() D����ˮ�м�������NH4Cl��
D����ˮ�м�������NH4Cl��![]() ���ˮ�������OHһ����ˮ�������c(H+)>l��10-7mol��L
���ˮ�������OHһ����ˮ�������c(H+)>l��10-7mol��L
 ���㼤�������100�ִ��Ծ�ϵ�д�
���㼤�������100�ִ��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
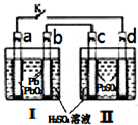 �ɻ�����������������̹�ˣ�������������Ϊ������Դ�ǵ��͵Ŀɳ��͵�أ��ܷ�ӦʽΪ��
�ɻ�����������������̹�ˣ�������������Ϊ������Դ�ǵ��͵Ŀɳ��͵�أ��ܷ�ӦʽΪ��
| ||
| ��� |
| ʵ������ | ʵ�鷽�� | ʵ������ԭ����� |
| �ٵ�����Ũ�������ƽ���Ӱ�� | ȡPbI2������Һ������һ֧�Թ��У��ټ�������NaI������Һ�� ȡPbI2������Һ������һ֧�Թ��У��ټ�������NaI������Һ�� |
��Һ�г��ֻ�ɫ���ǣ� ԭ������Һ��c��I-������ʹQc������pbI2��Ksp ��Һ�г��ֻ�ɫ���ǣ� ԭ������Һ��c��I-������ʹQc������pbI2��Ksp |
| ��Ǧ����Ũ�ȼ�С��ƽ���Ӱ�� | ȡPbI2����Һ������һ֧�Թ��У��ټ�������NaCl������Һ ȡPbI2����Һ������һ֧�Թ��У��ټ�������NaCl������Һ |
��ɫ������ʧ ԭ�����γ�PbCl42-��������Һ��c��Pb2+����С��ʹQcС����pbI2��Ksp ��ɫ������ʧ ԭ�����γ�PbCl42-��������Һ��c��Pb2+����С��ʹQcС����pbI2��Ksp |
| �� Ǧ���Ӻ͵�����Ũ�ȶ���С��ƽ���Ӱ�� Ǧ���Ӻ͵�����Ũ�ȶ���С��ƽ���Ӱ�� |
��PbI2����Һ�м�������FeCl3������Һ | PbI2 +2Fe3++4Cl-=PbCl42-+2Fe2++I2 PbI2 +2Fe3++4Cl-=PbCl42-+2Fe2++I2 |
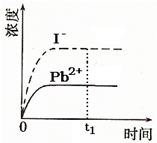 ����֪������PbI2��Ksp=8.0��10-9��������PbI2�������� 100mLˮ�����պñ��ͣ��ù�����Pb2+��I-Ũ����ʱ��仯��ϵ��ͼ������PbI2��Һ��c��I-��=0.0025mol?L-1������t1ʱ����������ϵ�м���100mL����0.020mol?L-1 NaI ��Һ������t1ʱ�̺�Pb2+��I-Ũ����ʱ��仯��ϵͼ��
����֪������PbI2��Ksp=8.0��10-9��������PbI2�������� 100mLˮ�����պñ��ͣ��ù�����Pb2+��I-Ũ����ʱ��仯��ϵ��ͼ������PbI2��Һ��c��I-��=0.0025mol?L-1������t1ʱ����������ϵ�м���100mL����0.020mol?L-1 NaI ��Һ������t1ʱ�̺�Pb2+��I-Ũ����ʱ��仯��ϵͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�걱�������ƶ��и߶����£����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��������ĩ�� ���ͣ���ѡ��
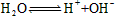 ������������ȷ����
������������ȷ�����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com