
| A����Ӧ��ƽ��ʱN2��ת����Ϊ10% |
| B����Ӧ���е�10 sĩʱ��H2��ƽ����Ӧ������0.03 mol��(L��s)��1 |
| C���÷�Ӧ�ﵽƽ��ʱ��N2��ƽ��Ũ��Ϊ0.45 mol/L |
| D���÷�Ӧ�ﵽƽ��ʱ��ѹǿ����ʼʱѹǿ��0.95�� |
 2NH3����c(N2)��0.45mol��L��1�����ĵ�N2Ϊ0.1mol�����Է�Ӧ��ƽ��ʱN2��ת����Ϊ10%������c(H2)��0.15mol��L��1���Է�Ӧ���е�10 sĩʱ��H2��ƽ����Ӧ������0.015 mol��(L��s)��1����B����Ӧ��ƽ��ʱ���ܵ����ʵ���Ϊ3.8mol����Ӧǰ�е����ʵ���Ϊ4mol���������Ը÷�Ӧ�ﵽƽ��ʱ��ѹǿ����ʼʱѹǿ��0.95�����ʴ����һ����B�ѡB ��
2NH3����c(N2)��0.45mol��L��1�����ĵ�N2Ϊ0.1mol�����Է�Ӧ��ƽ��ʱN2��ת����Ϊ10%������c(H2)��0.15mol��L��1���Է�Ӧ���е�10 sĩʱ��H2��ƽ����Ӧ������0.015 mol��(L��s)��1����B����Ӧ��ƽ��ʱ���ܵ����ʵ���Ϊ3.8mol����Ӧǰ�е����ʵ���Ϊ4mol���������Ը÷�Ӧ�ﵽƽ��ʱ��ѹǿ����ʼʱѹǿ��0.95�����ʴ����һ����B�ѡB ��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 eC��g����fD��g���ڷ�Ӧ�����У���������������ʱ��C���������
eC��g����fD��g���ڷ�Ӧ�����У���������������ʱ��C��������� ��C���ڲ�ͬ�¶ȣ�T���Ͳ�ͬѹǿ��P������������ʱ�䣨t���ı仯��ϵ��ͼ��ʾ������������ȷ���� �� ��
��C���ڲ�ͬ�¶ȣ�T���Ͳ�ͬѹǿ��P������������ʱ�䣨t���ı仯��ϵ��ͼ��ʾ������������ȷ���� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| A���÷�Ӧ��ֹͣ |
| B����λʱ���ڵ������������ʵ����������������� |
| C��3v(H2)=2v(NH3) |
| D��c(H2) ��c(N2) ��c(NH3) =" 7" ��9 ��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
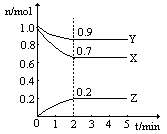
 nY��g������H =QkJ/mol����Ӧ�ﵽƽ��ʱ��Y�����ʵ���Ũ�����¶ȡ���������Ĺ�ϵ���±���ʾ��
nY��g������H =QkJ/mol����Ӧ�ﵽƽ��ʱ��Y�����ʵ���Ũ�����¶ȡ���������Ĺ�ϵ���±���ʾ��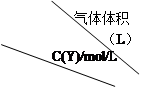 �¶ȡ� | 1 | 2 | 3 |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.09 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2SO3(g)��һ�������´ﵽƽ�⣬���c(SO3)��0.040mol��L-1������������·�Ӧ��ƽ�ⳣ��K��SO2��ƽ��ת���� �� ��
2SO3(g)��һ�������´ﵽƽ�⣬���c(SO3)��0.040mol��L-1������������·�Ӧ��ƽ�ⳣ��K��SO2��ƽ��ת���� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NO2�SH<0��Ӧ��NO��ת�������¶ȵĹ�ϵ���ߣ�
2NO2�SH<0��Ӧ��NO��ת�������¶ȵĹ�ϵ���ߣ�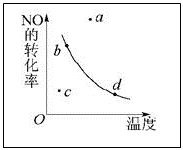
| A��a�� | B��b�� | C��c�� | D��d�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO(g)��H2(g)������H2O��CO�����ʵ�����mol����ʱ�䣨min���ı仯��������ͼ��ʾ��
CO(g)��H2(g)������H2O��CO�����ʵ�����mol����ʱ�䣨min���ı仯��������ͼ��ʾ��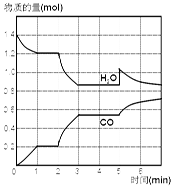
| A��������C | B��������ˮ���� | C���������¶� | D��������ѹǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 Ag��(aq)��Cl��(aq) ��25��ʱ��AgCl��Ksp��1.8��10��10���ֽ�����AgCl�ֱ��������Һ���У���100 mL����ˮ����100 mL 0.3 mol��L��1 AgNO3��Һ����100 mL 0.1 mol��L��1MgCl2��Һ��ֽ������ȴ����ͬ�¶ȣ�Ag��Ũ���ɴ�С��˳��Ϊ__________________(�����)����ʱ��Һ����Cl�����ʵ���Ũ��Ϊ__________________��
Ag��(aq)��Cl��(aq) ��25��ʱ��AgCl��Ksp��1.8��10��10���ֽ�����AgCl�ֱ��������Һ���У���100 mL����ˮ����100 mL 0.3 mol��L��1 AgNO3��Һ����100 mL 0.1 mol��L��1MgCl2��Һ��ֽ������ȴ����ͬ�¶ȣ�Ag��Ũ���ɴ�С��˳��Ϊ__________________(�����)����ʱ��Һ����Cl�����ʵ���Ũ��Ϊ__________________���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com