
һ���¶��£������Ϊ2L�ĺ����ܱ������г���1mol PCl5(g)��������Ӧ��PCl5(g) PCl3(g)+Cl2(g) ��H=+Q KJ/molά�������¶Ȳ��䣬���������ѹǿ�淴Ӧʱ��ı仯��ͼ��ʾ������˵����ȷ���ǣ� ��
PCl3(g)+Cl2(g) ��H=+Q KJ/molά�������¶Ȳ��䣬���������ѹǿ�淴Ӧʱ��ı仯��ͼ��ʾ������˵����ȷ���ǣ� ��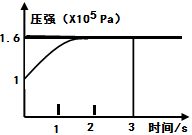
| A��3s�ڵ�ƽ������Ϊ��V��PCl3��=0.1mol��L-1��min-1 |
| B���ﵽƽ��ʱ�ų�0.6QKJ���� |
| C�������������䣬���������г���1molPCl5(g)�������ƽ�� ʱ��C(PCl5)��0.4mol��L-1 |
| D�������������䣬����PCl5��Ũ�ȣ�ƽ�ⳣ����С |
C
������������� A�����¡����ݵ��ܱ������У���������ʵ���֮�ȵ���ѹǿ֮�ȣ���ƽ��ʱ�����������ʵ���Ϊ1.6mol����������ʵ�������1.6-1��mol=0.6mol��������PCl3�����ʵ���Ϊx��
PCl5��g��?PCl3��g��+Cl2��g�� �������ӵ����ʵ���
1mol 1mol
x 0.6mol
x= mol=0.6mol��
mol=0.6mol��
V��PCl3��==0.1mol/��L��s����ʱ�䵥λ��S����min������B���÷�Ӧ�����ȷ�Ӧ���Ƿ��ȷ�Ӧ������������1molʱ���յ�������QKJ������������0.6molʱ���յ�������0.6QKJ������ C��ƽ����ϵ���ټ���1mol��PCl5�����µ���ƽ��״̬�����Ե�ЧΪ��ʼ����2mol��PCl5���������Ϊԭ����2������ƽ�⣨��ƽ����ԭƽ���Ч�����ٽ����ѹ����ԭ����С����ԭƽ����ȣ�ѹǿ����ƽ�����淴Ӧ�����ƶ�����ƽ��Ũ�ȴ���ԭ������������ȷ��D���¶Ȳ��䣬ƽ�ⳣ�����䣬����
���㣺 ��ѧƽ���Ӱ������


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��Ӧ3X(g)+Y(g)  2Z(g)+2W(g)��2L�ܱ������н��У�5min��Y������0.5mol����˷�Ӧ������vΪ( )
2Z(g)+2W(g)��2L�ܱ������н��У�5min��Y������0.5mol����˷�Ӧ������vΪ( )
| A��v(X)=0.05mol��L�C1��min�C1 | B��v(Z)=0.10mol��L�C1��min�C1 |
| C��v(Y)=0.10mol��L�C1��min�C1 | D��v(W)=0.05mol��L�C1��min�C1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������ʵ��������������ԭ�����͵��ǣ� ��
A����ˮ����ƽ�⣺Cl2+H2O HCl+HClO��������AgNO3��Һ����Һ��ɫ��dz HCl+HClO��������AgNO3��Һ����Һ��ɫ��dz |
B����CO(g)+NO2(g) CO2(g)+NO(g)��ƽ����ϵ����ѹǿ��ʹ��ɫ���� CO2(g)+NO(g)��ƽ����ϵ����ѹǿ��ʹ��ɫ���� |
C����2NO2(g)  N2O4(g), �����¶�ƽ����ϵ��ɫ���� N2O4(g), �����¶�ƽ����ϵ��ɫ���� |
| D��SO2��������SO3�ķ�Ӧ��������������Ŀ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ݻ���ͬ��A��B�����ܱ������У��ֱ����2molSO2��1molO2��ʹ��������ͬ�¶��·�����Ӧ��2SO2+O2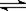 2SO3���ﵽƽ�⡣�ڷ�Ӧ�����У���A��������������䣬B��������ѹǿ���䣬�� A �е� SO2 ��ת����Ϊ 25% ʱ���� B ������ SO2 ��ת����Ӧ��
2SO3���ﵽƽ�⡣�ڷ�Ӧ�����У���A��������������䣬B��������ѹǿ���䣬�� A �е� SO2 ��ת����Ϊ 25% ʱ���� B ������ SO2 ��ת����Ӧ��
A��25% B������25% C����25% D��12.5%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪ (CH3COOH)2 (g)  2CH3COOH(g)����ʵ���ò�ͬѹǿ�£���ϵ��ƽ��Ħ��������
2CH3COOH(g)����ʵ���ò�ͬѹǿ�£���ϵ��ƽ��Ħ��������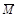 =
=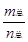 �����¶ȣ�T���ı仯������ͼ��ʾ������˵����ȷ����
�����¶ȣ�T���ı仯������ͼ��ʾ������˵����ȷ����
| A���ù��̵ġ�H < 0 |
| B������ѹǿ��P(a) < P(b) = P(c) |
| C��ƽ�ⳣ����K(a) =" K(b)" < K(c) |
| D���ⶨ�������Է�������Ҫ�ڸ�ѹ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ�������£��ֱ����ݻ��̶����ܱ������г���A������B��������Ӧ���£�2A(g)+B(s) 2D(g)��H��0,�������������£�������֪����˵������ȷ����
2D(g)��H��0,�������������£�������֪����˵������ȷ����
| | ʵ��� | ʵ��� | ʵ��� |
| ��Ӧ�¶�/�� | 800 | 800 | 850 |
| c(A)��ʼ/mol��L��1 | 1 | 2 | 1 |
| c(A)ƽ��/mol��L��1 | .0.5 | 1 | 0.85 |
| �ų�������/kJ | a | b | c |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
COCl2(g) CO(g)+Cl2(g)�� ��H��0 ����Ӧ�ﵽƽ��ʱ�����д�ʩ�������� �ں���ͨ��������� ������CO��Ũ�� �ܼ�ѹ �ݼӴ��� ��ѹͨ��������壬�����COCl2ת���ʵ���
CO(g)+Cl2(g)�� ��H��0 ����Ӧ�ﵽƽ��ʱ�����д�ʩ�������� �ں���ͨ��������� ������CO��Ũ�� �ܼ�ѹ �ݼӴ��� ��ѹͨ��������壬�����COCl2ת���ʵ���
| A���٢ڢ� | B���٢ܢ� | C���ڢۢ� | D���ۢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ�������£���2L�ܱ������м���ijA����8.0mol����4sʱ���A��������ʵ���Ϊ5.6mol�����4s����A��ʾ�÷�Ӧ������ȷ���ǣ� ( )
| A��0.3 mol��L-1s-1 | B��0.6 mol��L-1s-1 |
| C��1.0 mol��L-1s-1 | D��0.7 mol��L-1s-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ܱ�������ͨ�����ʵ���Ũ�Ⱦ�0.1mol��L-1��CH4��CO2����һ�������·�����Ӧ�� �����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ5�������й�˵��һ����ȷ����
�����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ5�������й�˵��һ����ȷ����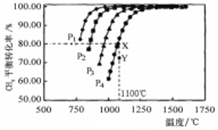
| A��������Ӧ�ġ�H>0 |
| B��ѹǿP1>P2>P3>P4 |
| C��1100��÷�Ӧ��ƽ�ⳣ��Ϊ64mol2��L-1 |
| D��ѹǿΪP4ʱ����Y�㣺v(��)<v(��) |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com