
【题目】如图所示是Zn和Cu形成的原电池,其实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( ) 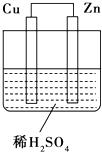
试验后的记录:
①Cu为负极,Zn为正极
②Cu极上有气泡产生
③SO42﹣向Cu移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子的流向是:Cu→Zn
⑥正极反应式:Cu﹣2e﹣=Cu2+ .
A.①②③
B.②④
C.④⑤⑥
D.③④⑤
【答案】B
【解析】解:①在该原电池中,活泼金属锌做负极,金属铜做正极,故①错误;②根据金属活动性顺序知,锌作负极,铜作正极,氢离子在铜电极上得电子生成氢气,发生还原反应,所以在铜极上有气泡产生,发生还原反应,故②正确;
③锌失去电子变成金属阳离子进入溶液,所以在锌极附近有带正电荷的离子,根据异性电荷相吸原理,硫酸根离子向锌极移动,故③错误;
④根据电极反应式:2H++2e﹣=H2↑
2mol 1mol
0.5mol0.25mol
故④正确;
⑤外电路电子流向为从负极到正极,即Zn→Cu,故⑤错误;
⑥正极上氢离子得电子生成氢气,所以其反应式为 2H++2e﹣=H 2↑,故⑥错误.
故选B.


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
【题目】下列关于下图实验装置的说法正确的是( )
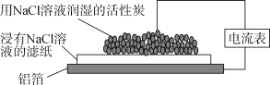
A.该装置电流表中没有电流通过
B.铝箔是正极
C.总反应为4Al+3O2+6H2O===4Al(OH)3
D.电子从铝箔流出,经电流表、活性炭、滤纸回到铝箔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A的单质可形成气态分子X,X的水溶液呈碱性;D的简单阳离子与X具有相同的电子数,且D是同周期元素中原子半径最大的元素;E元素的原子最外层比次外层少两个电子,C、F两种元素的原子最外层共有13个电子。则
(1)X的电子式为___________。
(2)B单质的结构式为___________;用电子式表示E的气态氢化物的形成过程:___________________________。
(3)C与D形成的两种化合物中,其中一种物质含有两种类型的化学键,该物质属于________(填“离子化合物”或“共价化合物”)。
(4)B、C、E分别与A形成的化合物中最稳定的是______(写结构式)。
(5)D是同周期简单阳离子中离子半径最____的元素。
(6)F的单质在反应中常作________剂(填“氧化”或“还原”)。F的单质与水反应的离子方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D是中学化学中常见的四种不同粒子,它们之间存在如图所示的转化关系(反应条件已经略去):
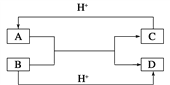
(1)如果A、B、C、D均是10电子的粒子,请写出A、D的电子式:A_________;D_______。
(2)如果A和C是18电子的粒子,B和D是10电子的粒子,请写出:A与B在溶液中反应的离子方程式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为( )
A. a g·mol-1B. a gC. 50a g·mol-1D. 50a g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写不正确的是( )
A.Fe与HCl反应:2Fe+6H+═2Fe3++3H2↑
B.Cu与AgNO3反应:2Ag++Cu═Cu2++2Ag
C.醋酸与NaOH反应:CH3COOH+OH﹣═CH3COO﹣+H2O
D.CuSO4与Ba(OH)2反应:Cu2++2OH﹣+SO ![]() +Ba2+═BaSO4↓+Cu(OH)2↓
+Ba2+═BaSO4↓+Cu(OH)2↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com