

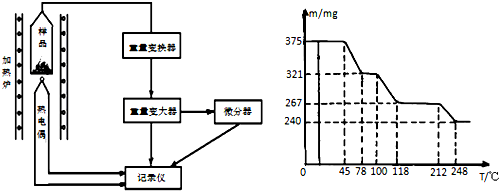
·ÖĪö æ×ČøŹÆµÄÖ÷ŅŖ³É·ÖŹĒCuCO3•Cu£ØOH£©2£¬»¹ŗ¬ÓŠÉŁĮæµÄSiO2ŗĶĢśµÄ»ÆŗĻĪļ£¬¼ÓČė¹żĮæĻ”ĮņĖį£¬Éś³ÉĒāĘųAĪŖ¶žŃõ»ÆĢ¼ĘųĢ壬ČÜŅŗBŗ¬ÓŠĮņĖįĶ”¢ĮņĖįŃĒĢśµČ£¬¼ÓČė¹żŃõ»ÆĒā£¬·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬ČÜŅŗCÖŠŗ¬ÓŠĮņĖįĶ”¢ĮņĖįĢśµČ£¬¼ÓČėCuOæɵ÷½ŚČÜŅŗpH£¬ĄūÓŚĢśĄė×ÓµÄĖ®½ā¶ųÉś³ÉĒāŃõ»ÆĢś³Įµķ£¬ČÜŅŗDŗ¬ÓŠĮņĖįĶ£¬¾Õō·¢”¢½į¾§æɵƵ½ĮņĖįĶ¾§Ģ壬
£Ø1£©ŃĒĢśĄė×Ó¾ßÓŠ»¹ŌŠŌ£¬Äܱ»øßĆĢĖį¼ŲŃõ»ÆĪŖČż¼ŪĢś£¬Ź¹øßĆĢĖį¼ŲĶŹÉ«£»
£Ø2£©øł¾ŻH2O2+2Fe2++2H+=2Fe3++2H20µÄ²śĪļ½ā“š£»
£Ø3£©“ÓČÜŅŗÖŠŅŖĪö³ö¾§Ģ壬²ÉÓĆĄäČ“½į¾§·Ø£»¹żĀĖŹ±ŅŖÓƵ½²£Į§°ōŅżĮ÷£»
£Ø4£©ÓÉĶ¼ĻóÖŠĪļÖŹµÄ±ä»ÆĒéæö·ÖĪöĮņĖįĶ¾§Ģå·Ö½āµÄ×īµĶĪĀ¶Č£¬ŅĄ¾Ż212-250”ęĪĀ¶Č·¶Ī§ÄŚ¹ĢĢåĪļÖŹµÄÖŹĮæŹż¾Ż½ųŠŠ·ÖĪö¼“æÉ£¬ŅĄ¾ŻŠÅĻ¢ÖŠ¹ŲÓŚ·“Ó¦µÄŠšŹöŹéŠ“·½³ĢŹ½¼“æÉ£®
½ā“š ½ā£ŗ£Ø1£©ŃĒĢśĄė×Ó¾ßÓŠ»¹ŌŠŌ£¬Äܱ»øßĆĢĖį¼ŲŃõ»ÆĪŖČż¼ŪĢśĄė×Ó£¬Ź¹øßĆĢĖį¼ŲĶŹÉ«£¬ŹĒ¼ģŃéČÜŅŗAÖŠFe2+µÄ×ī¼ŃŹŌ¼Į£¬
¹Ź“š°øĪŖ£ŗa£»
£Ø2£©H2O2¾ßÓŠŃõ»ÆŠŌ£¬ŌŚøĆ·“Ó¦ÖŠ×÷Ńõ»Æ¼Į£¬ŃĒĢśĄė×Ó¾ßÓŠ»¹ŌŠŌ£¬·¢ÉśH2O2+2Fe2++2H+=2Fe3++2H20£¬H2O2ÓėFe2+·“Ӧɜ³ÉµÄH20ĪŖČܼĮĪŽĪŪČ¾£¬²»»įŅżČėŠĀµÄŌÓÖŹĄė×Ó£¬
¹Ź“š°øĪŖ£ŗH2O2+2Fe2++2H+=2Fe3++2H20£»²»»įŅżČėŠĀµÄŌÓÖŹĄė×Ó£»
£Ø3£©ÓÉČÜŅŗÖĘČ”¾§Ģ壬Šč¾¹ż¼ÓČČÅØĖõ£¬ĄäČ“½į¾§²ÅæɵƵ½£¬ŌŚ¹żĀĖ²Ł×÷ÖŠ£¬³żÉÕ±”¢²£Į§°ō”¢½ŗĶ·µĪ¹ÜĶā£¬»¹ŠčµÄŅ»ÖÖ²£Į§ŅĒĘ÷ŹĒ²£Į§°ō£¬ĖüµÄ×÷ÓĆŹĒŅżĮ÷£¬
¹Ź“š°øĪŖ£ŗĄäČ“½į¾§£»ŅżĮ÷£»
£Ø4£©ÓÉĶ¼·ÖĪöæÉÖŖ£¬CuSO4•5H2OŹÜČȵ½45”ꏱæŖŹ¼ĶŃĖ®·Ö½ā£¬212”ꏱæɵƵ½½ĻĪČ¶ØµÄŅ»ÖÖÖŠ¼äĪļ£¬ŌŚ212”ꏱŹ§Č„µÄĖ®µÄÖŹĮæĪŖ0.375g-0.267g=0.108g£¬øł¾Ż·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
CuSO4•5H2O$\frac{\underline{\;\;”÷\;\;}}{\;}$CuSO4•£Ø5-n£©H2O+nH2O
250 18n
0.375g 0.108g
½āµĆn=4£¬212”ꏱæɵƵ½½ĻĪČ¶ØµÄŅ»ÖÖÖŠ¼äĪļĪŖCuSO4•H2O
248”ꏱæɵƵ½½ĻĪČ¶ØµÄŅ»ÖÖÖŠ¼äĪļ£¬øł¾Ż·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
CuSO4•H2O$\frac{\underline{\;\;”÷\;\;}}{\;}$CuSO4•£Ø1-n£©H2O+nH2O
178 18n
0.267g 0.267g-0.240g=0.027g
½āµĆn=1£¬248”ꏱæɵƵ½½ĻĪČ¶ØµÄŅ»ÖÖÖŠ¼äĪļĪŖCuSO4£¬212-250”ęĪĀ¶Č·¶Ī§ÄŚ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖCuSO4•H2O$\frac{\underline{\;\;”÷\;\;}}{\;}$CuSO4+H2O£¬
¹Ź“š°øĪŖ£ŗCuSO4•H2O$\frac{\underline{\;\;”÷\;\;}}{\;}$CuSO4+H2O£®
µćĘĄ ±¾Ģā漲鳣¼ū½šŹōµÄµ„ÖŹ¼°Ęä»ÆŗĻĪļµÄÓ¦ÓĆŗĶĮņĖįĶ½į¾§Ė®ŗ¬ĮæµÄ²ā¶Ø£¬ÕĘĪÕĪļÖŹµÄÖĘČ”ŗĶĢį“攢Ąė×ӵļģŃéµČŹµŃé²Ł×÷£¬·ÖĪöĶ¼ĻóŠÅĻ¢ŹĒĶź³É±¾ĢāÄæµÄ¹Ų¼ü£¬ĢāÄæ½ĻĪŖ×ŪŗĻ£¬ÄѶČÖŠµČ£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
 ČēĶ¼ŹĒ²”ČĖŹäŅŗÓƵÄĘĻĢŃĢĒ£Ø·Ö×ÓŹ½ĪŖC6H12O6£©×¢ÉäŅŗµÄ±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ£®¾Ż±źĒ©ĖłĢį¹©µÄŠÅĻ¢£¬ŅŌĻĀĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
ČēĶ¼ŹĒ²”ČĖŹäŅŗÓƵÄĘĻĢŃĢĒ£Ø·Ö×ÓŹ½ĪŖC6H12O6£©×¢ÉäŅŗµÄ±źĒ©ÉĻµÄ²æ·ÖÄŚČŻ£®¾Ż±źĒ©ĖłĢį¹©µÄŠÅĻ¢£¬ŅŌĻĀĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | øĆ×¢ÉäŅŗÖŠĘĻĢŃĢĒµÄÖŹĮæ·ÖŹżŹĒ5% | |
| B£® | ĘĻĢŃĢĒµÄĦ¶ūÖŹĮæĪŖ180g•mol-1 | |
| C£® | øĆ×¢ÉäŅŗµÄĆܶČŌ¼ĪŖ1g•mL-1 | |
| D£® | øĆ×¢ÉäŅŗÖŠĘĻĢŃĢĒµÄĪļÖŹµÄĮæÅضČŌ¼ĪŖ0.014 mol•L-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| »ÆѧŹ½ | µēĄėĘ½ŗā³£Źż£Ø25”ę£© |
| HCN | K=4.9”Į10-10 |
| CH3COOH | K=1.8”Į10-5 |
| H2CO3 | K1=4.3”Į10-7 K2=5.6”Į10-11 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| µĪ¶Ø“ĪŹż | “ż²āŅŗĢå»ż/mL | ±ź×¼ŃĪĖįĢå»ż£ØmL£© | |
| µĪ¶ØĒ°¶ĮŹż£ØmL£© | µĪ¶Øŗó¶ĮŹż£ØmL£© | ||
| µŚŅ»“Ī | 10.00 | 0.50 | 20.40 |
| µŚ¶ž“Ī | 10.00 | 4.00 | 24.10 |
| µŚČż“Ī | 10.00 | 4.20 | 26.70 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·Å³ö¼īŅŗµÄµĪ¶Ø¹ÜæŖŹ¼ÓŠĘųÅŻ£¬·¢³öŅŗĢåŗóĘųÅŻĻūŹ§ | |
| B£® | µĪ¶Ø¹ÜÓĆÕōĮóĖ®Ļ“µÓŗó£¬Ö±½Ó×¢Čė±ź×¼ĖįŅŗ½ųŠŠµĪ¶Ø | |
| C£® | ׶ŠĪĘæÓĆÕōĮóĖ®Ļ“µÓŗó£¬Ö±½Ó¼ÓČė“ż²āČÜŅŗµĪ¶Ø | |
| D£® | µĪ¶Ø¹ÜÓĆÕōĮóĖ®Ļ“µÓŗó£¬Ö±½Ó×¢Čė“ż²āŅŗ£¬Č”20.00 mL½ųŠŠµĪ¶Ø |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČĪŗĪĢõ¼žĻĀ£¬·“Ó¦2CO2£Øg£©ØT2CO£Øg£©+O2£Øg£©¾ł²»ÄÜ×Ō·¢½ųŠŠ | |
| B£® | ŅĄ¾Ż·“Ó¦I2+2S2O32-ØT2I-+S4O62-£¬ČōŅŖ²ā¶ØĘ½ŗāĢåĻµI2+I-?I3-ÖŠĘ½ŗāŹ±µÄ c£ØI2£©£¬æÉÓĆŅŃÖŖĪļÖŹµÄĮæÅØ¶ČµÄNa2S2O3ČÜŅŗ½ųŠŠµĪ¶ØŹµŃé | |
| C£® | Ļņŗ¬ÓŠ±½·ÓµÄ±½ČÜŅŗÖŠµĪČėÉŁĮæÅØäåĖ®Ī“¼ū°×É«³Įµķ£¬ŹĒŅņĪŖÉś³ÉµÄČżäå±½·ÓÓÖČÜÓŚ±½ÖŠ | |
| D£® | ¼ģŃéijĪļÖŹŹĒ·ńŗ¬ÓŠFe2O3µÄ²Ł×÷²½ÖčŹĒ£ŗѳʷ·ŪĖ锜¼ÓĖ®Čܽā”ś¹żĀĖ£¬ĻņĀĖŅŗÖŠµĪ¼ÓKSCNČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | Ī¢Į£×é | Ėł¼ÓŹŌ¼Į | Ąė×Ó·½³ĢŹ½ |
| A | NH4+”¢Mg2+”¢SO42- | ÉŁĮæBa£ØOH£©2ČÜŅŗ | NH4++SO42-+Ba2++OH-=BaSO4”ż+NH3•H2O |
| B | Mg2+”¢HCO3-”¢Cl- | ¹żĮæNaOHČÜŅŗ | Mg2++2HCO3-+2OH-=MgCO3-”ż+CO32-+2H2O |
| C | H+”¢Na+”¢NO3- | Fe·Ū | Fe+2H+=Fe2++H2”ü |
| D | Ca2+”¢NH3•H2O”¢Cl- | ĶØČė¹żĮæCO2 | NH3•H2O+CO2=NH4++HCO3- |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com