
【题目】有机物AH的转化关系如下图所示。其中A是植物生长调节剂,它的产量可以用来衡量一个国家的石油化工发展水平;D是一种合成高分子材料,此类物质如果大量使用易造成“白色污染”。

请回答下列问题:
(1)E官能团的电子式为_____。
(2)关于有机物A、B、C、D的下列说法,不正确的是____(选填序号)。
a. A、B、C、D均属于烃类
b. B的同系物中,当碳原子数≥4时开始出现同分异构现象
c. 等质量的A和D完全燃烧时消耗O2的量相等,生成CO2的量也相等
d. B不能使溴水或酸性高锰酸钾溶液褪色,但A和D可以
(3)写出下列反应的化学方程式:
反应③:____________________________;
反应⑥:_____________________________。
(4)C是一种速效局部冷冻麻醉剂,可由反应①或②制备,请指出用哪一个反应制备较好:_______,并说明理由:__________________。
【答案】![]() ad nCH2=CH2
ad nCH2=CH2![]()
![]() CH3COOH+CH3CH2OH
CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O ① 反应①为加成反应,原子利用率100%,反应②为取代反应,有副反应,CH3CH2Cl产量较低,故反应①制备较好
CH3COOCH2CH3+H2O ① 反应①为加成反应,原子利用率100%,反应②为取代反应,有副反应,CH3CH2Cl产量较低,故反应①制备较好
【解析】
A是植物生长调节剂,它的产量用来衡量一个国家石油化工发展的水平,即A为乙烯,结构简式为CH2=CH2;A与H2发生加成,即B为CH3CH3;A与HCl发生加成反应,即C为CH3CH2Cl;A与H2O发生加成反应,即E为CH3CH2OH;反应⑤是乙醇的催化氧化,即F为CH3CHO;乙醇被酸性K2Cr2O7氧化成乙酸,即G为CH3COOH;乙醇与乙酸发生酯化反应,生成H,则H为CH3CH2OOCCH3;D为高分化合物,常引起白色污染,即D为聚乙烯,其结构简式为![]() ,据此分析;
,据此分析;
(1)根据上述分析,E为CH3CH2OH,其官能团是-OH,电子式为![]() ;
;
(2)a、A、B、C、D结构简式分别是CH2=CH2、CH3CH3、CH3CH2Cl、![]() ,其中C不属于烃,故a说法错误;
,其中C不属于烃,故a说法错误;
b、烷烃中出现同分异构体,当碳原子≥4时开始出现同分异构现象,故b说法正确;
c、A和D的最简式相同,因此等质量时,耗氧量相同,故c说法正确;
d、B为乙烷,不能使酸性高锰酸钾溶液或溴水褪色,D中不含碳碳双键,也不能使酸性高锰酸钾溶液或溴水褪色,故d说法错误;
答案选ad;
(3)反应③发生加聚反应,其反应方程式为nCH2=CH2![]()
![]() ;
;
反应⑥发生酯化反应,反应方程式为CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(4)反应①为加成反应,原子利用率100%,反应②为取代反应,有副反应,CH3CH2Cl产量较低,故反应①制备较好。


科目:高中化学 来源: 题型:
【题目】![]() 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
A. 0.1 mol 的![]() 中,含有
中,含有![]() 个中子
个中子
B. pH=1的H3PO4溶液中,含有![]() 个
个![]()
C. 2.24L(标准状况)苯在O2中完全燃烧,得到![]() 个CO2分子
个CO2分子
D. 密闭容器中1 mol PCl3与1 mol Cl2反应制备 PCl5(g),增加![]() 个P-Cl键
个P-Cl键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,HNO2和CH3COOH的电离常数分別为5.0×10-4和1.7×10-5。将pH和体积均相同的两种酸溶液分别稀释,其pH随加水体积的变化如图所示。下列叙述正确的是

A.曲线I代表HNO2溶液
B.溶液中水的电离程度:b点>c点
C.相同体积a点的两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
D.从c点到d点,溶液中![]() 保持不变(其中HA、A-分别代表相应的酸和酸根离子)
保持不变(其中HA、A-分别代表相应的酸和酸根离子)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钕铁硼磁铁是目前为止具有最强磁力的永久磁铁。预计在未来20年里,不可能有替代钕铁硼磁铁的磁性材料出现。生产钕铁硼磁铁的主要原材料有稀土金属钕、纯铁、铝、硼以及其它稀土原料。
(1) 钕(Nd)为60号元素,在元素周期表中的位置是_____;基态铁原子的外围电子排布图是______。
(2)实验测得气态A1C13的实际存在形式为A12C16双聚分子,其中A1原子的杂化方式是__________;A12C16与过量NaOH溶液反应生成Na[Al(OH)4];[A1(OH)4]-中存在的化学键有______(填选项字母)。
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
(3)已知立方BN晶体硬而脆,其原因是_______;其晶胞结构如图所示,N原子填充在B原子构成的正四面体空隙中,则晶胞中正四面体的空隙填充率为_______,设晶胞中最近的B、N原子之间的距离为a nm,晶体的密度为b gcm-3,则阿伏加德罗常数为_____mol-1 (列式即可,用含a、b的代数式表示)
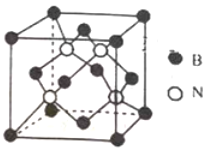
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列为某学生在实验室中制备高锰酸钾晶体的流程图。
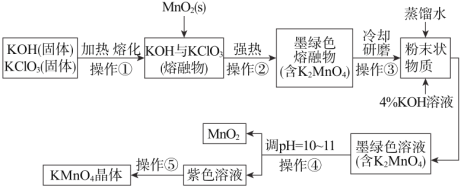
根据上图回答下列问题:
(1)操作①和②均需在坩埚中进行,根据实验实际应选择坩埚为_____(填字母);
a.石英坩埚 b.氧化铝坩埚 c.铁坩埚
(2)已知:3MnO42-+2H2O2MnO4-+MnO2+4OH-。操作④中通CO2调pH=10~11,其目的是_____;
(3)得到墨绿色溶液后,也可用如图所示方法制备KMnO4,电极均为铂电极。
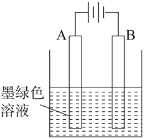
①A极上的电极反应式为_____;
②这种方法与上面的方法相比,其优点是_____;
(4)实验室中,可用0.10mol/L,草酸作标准溶液,利用下述反应,测定所得KMnO4晶体的纯度。5H2C2O4+2KMnO4+3H2SO4=10CO2↑+2MnSO4+K2SO4+8H2O
取agKMnO4晶体样品配制成100mL溶液。每次取20.00mL于锥形瓶中进行滴定实验两次。两次实验所用草酸标准溶液的体积分别为22.15mL和22.17mL,由此求得KMnO4晶体的纯度为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质结构或性质的说法不正确的是( )
A.三联苯![]() 与四联苯
与四联苯![]() 互为同系物
互为同系物
B.可用燃烧法鉴别环乙烷、苯、CCl4
C.分子式为C5H10的烃存在顺反异构体
D.分子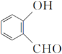 中所有原子可能位于同一平面
中所有原子可能位于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是()
A.1.0 mol·L-1的KNO3溶液:H+,Fe2+,Cl-,![]()
B.石蕊溶液呈红色的溶液:![]() ,Ba2+,
,Ba2+,![]() ,Cl-
,Cl-
C.pH=12的溶液:K+,Na+,CH3COO-,Br-
D.与铝反应产生大量氢气的溶液:Na+,K+,![]() ,
,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:用NH3催化还原NOx时包含以下反应.
反应①:4NH3 (g)+6NO(g) ![]() 5N2(g)+6H2O(l) H1=-1 807. 0 kJ·mol—1,
5N2(g)+6H2O(l) H1=-1 807. 0 kJ·mol—1,
反应②:4NH3(g)+6NO2(g) ![]() 5N2(g)+3O2(g)+6H2O(l) H2=?
5N2(g)+3O2(g)+6H2O(l) H2=?
反应③:2NO(g)+O2(g) ![]() 2NO2(g) H3=-113.0kJ·mol一1
2NO2(g) H3=-113.0kJ·mol一1
(1)反应②的H2==_____________。
(2)为探究温度及不同催化剂对反应①的影响.分别在不同温度、不同催化剂下.保持其他初始条件不变重复实验.在相同时间内测得N2浓度的变化情况如下图所示。

①反应①的平衡常数的表达式K=________。相同温度下.在催化剂甲的作用下反应的平衡常数______(填“大于”“小于”或“等于”)在催化剂乙的作用下反应的平衡常数。
②N点后N2浓度减小的原因可能是_____________________。
(3)某温度下,在1 L恒容密闭容器中初始投入4 mol NH3和6 mol NO发生反应①.当气体总物质的量为7.5mol时反应达到平衡.则NH3的转化率为____,达平衡所用时间为5 min.则用NO表示此反应0~5 min内的平均反应速率为______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为三套实验装置。

(1)写出下列仪器的名称:a.__________,b._____________。
(2)若利用装置1分离四氯化碳和酒精的混合物,还缺少的仪器是__________,将仪器补充完整后进行实验,冷凝水由________(填f或g) 口通入。
(3)用装置II分离混合物时,为使液体顺利流下,应进行的操作是_______________。
(4)实验室用Na2CO3·10H2O 晶体配制0.05mol/L 的Na2CO3 溶液970mL。
①应用托盘天平称取Na2CO3·10H2O 的质量是____g。
②装置III是某同学转移溶液的示意图。图中的错误是_______________。
③除了图中给出的仪器和托盘天平以及烧杯外,为完成实验还需要的仪器有:______________。
Ⅱ利用K2Cr2O7标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
(1)溶液配制:称取1.200 0 g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在________中溶解,完全溶解后,全部转移至100 mL的________中,加蒸馏水至________。
(2)滴定:取0.00950 mol·L-1的K2Cr2O7标准溶液20.00 mL,硫酸酸化后加入过量KI,发生反应:Cr2O72-+6I-+14H+===3I2+2Cr3++7H2O。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O32-===S4O62-+2I-。加入淀粉溶液作为指示剂,继续滴定,当溶液______,即为终点。平行滴定3次,样品溶液的平均用量为24.80 mL,则样品纯度为______%(保留1位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com