
| A、Al(OH)3既能够与盐酸反应又能够与NaOH溶液反应 |
| B、这种吸附剂也能吸附色素 |
| C、向Al2(SO4)3溶液中加入过量的NaOH溶液也能得到Al(OH)3 |
| D、实验室中Al(OH)3可以由可溶性铝盐溶液与足量的氨水反应制得 |


科目:高中化学 来源: 题型:
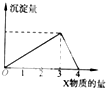 将X气体(或溶液)慢慢通入(或加人)一定量的Y溶液中,产生沉淀量与加入X的物质的量(mol)的关系如图所示,符合如图情况的是( )
将X气体(或溶液)慢慢通入(或加人)一定量的Y溶液中,产生沉淀量与加入X的物质的量(mol)的关系如图所示,符合如图情况的是( )| A、X为NaOH溶液,Y为AlCl3溶液 |
| B、X为CO2,Y为Ca(OH)2溶液 |
| C、X为NH3,Y为AlCl3溶液 |
| D、X为HCl溶液,Y为Na[Al(OH)4]溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾水解生成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| B、高温电解Al2O3可制得金属铝 |
| C、MgO的熔点很高,可用于制作耐高温材料 |
| D、根据冷的浓硫酸可以用铝质容器储存的事实,说明常温下铝不会与浓硫酸发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化铝可以用来制造耐火坩埚、耐火管和耐高温的实验仪器 |
| B、氢氧燃料电池、铅蓄电池、硅太阳能电池中都利用了原电池原理 |
| C、氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 |
| D、氨气溶于水显碱性,可以用湿润的红色石蕊试纸检验氨气的生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+、K+、Cl-、NO3- |
| B、Ba2+、Cl-、NH4+、HCO3- |
| C、Ag+、Na+、NO3-、Cl- |
| D、Al3+、SO42-、Cl-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com