
| A、往CH3COOH溶液中加水,c(OH-)和c(H+)均增大 |
| B、物质的量浓度均为0.1mol?1-1的CH3COOH溶液和NaOH溶液等体积混合,c(Na+)>(CH3COO-) |
| C、某浓度的氯化铵溶液中存在c(NH4+)>c(Cl-)>c(H+)>c(OH-) |
| D、在pH=4的氯化铵溶液中c(H+)+c(NH4+)=c(Cl-)+c(OH-) |


科目:高中化学 来源: 题型:
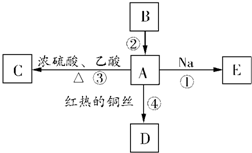 A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平.有关物质的转化关系如图所示:
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平.有关物质的转化关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③④① | B、④①②③ |
| C、①④②③ | D、③②①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有NA个氮原子的氮气在标准状况下的体积约为22.4 L |
| B、标准状况下,11.2 L H2O含有的分子数为0.5NA |
| C、在常温常压下,11.2 L Cl2含有的分子数为0.5NA |
| D、25℃,1.01×105Pa,64 g SO2中含有的原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、溶质的质量分数w%=
| ||
B、溶液密度ρ=
| ||
C、物质的量浓度c=
| ||
D、相对分子质量M=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L氧气做氧化剂时转移的电子数一定是4NA |
| B、1mol硝基(-NO2)与NA个二氧化氮(NO2)分子所含的电子数相等 |
| C、80 mL 12 mol/L的浓盐酸与足量MnO2反应,生成的Cl2分子数目为0.24NA |
| D、氧原子总数为0.2NA的SO2和O2的混合气体,其体积为2.24L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、取50ml该溶液,含硫酸的物质的量为10mol?L-1 |
| B、含硫酸的物质的量为0.5mol |
| C、含硫酸的物质的量为2mol?L-1 |
| D、含硫酸的物质的量为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两个原子之间形成共价键时,最多有一个σ键 |
| B、气体单质中,一定有σ键,可能有π键 |
| C、[Cu(NH3)4]2+和CH4两个粒子中中心原子Cu和C都是通过sp3杂化轨道成键 |
| D、中心原子采用sp2,该分子一定是平面三角形 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com