
分析 (1)氧气和臭氧是同素异形体,根据N=$\frac{m}{M}$NA、n=$\frac{m}{M}$结合分子构成进行计算;
(2)等温等压下,气体摩尔体积相等,相同体积的氧气和臭氧其物质的量相等,根据N=nNA、m=nM结合分子构成计算;
(3)根据ρ=$\frac{M}{{V}_{m}}$计算出该气体在标准状况下的密度;
(4)设需要稀硫酸的体积为xmL,然后根据稀释过程中硫酸的质量不变列式计算;
(5)电解质和非电解质都必须是化合物;电解质在熔融状态或水溶液中能导电的化合物,非电解质是在熔融状态和水溶液中都不能导电的化合物,金属单质能导电;电解质在熔融状态或水溶液中能导电,据此即可解答.
解答 解:①根据N=$\frac{m}{M}$NA知,相同质量时其分子数与摩尔质量成反比,所以二者分子数之比=48g/mol:32g/mol=3:2,根据分子构成知,其原子个数之比=(3×2):(2×3)=1:1,根据n=$\frac{m}{M}$知,相同质量时其物质的量等于摩尔质量反比=48g/mol:32g/mol=3:2,
故答案为:3:2;1:1;3:2;
②等温等压下,气体摩尔体积相等,相同体积的氧气和臭氧其物质的量相等,根据N=nNA知,分子数之比等于物质的量之比=1:1,根据分子构成知,其原子个数之比为2:3,根据m=nM知,相同物质的量时其质量之比等于摩尔质量之比=32g/mol:48g/mol=2:3,
故答案为:1:1;2:3;2:3.
(3)标准状况下气体摩尔体积约为22.4L/mol,该气体在标准状况下的密度ρ=$\frac{M}{{V}_{m}}$=$\frac{Mg/mol}{22.4L/mol}$=$\frac{M}{22.4}$g/L,
故答案为:$\frac{M}{22.4}$;
(4)配制100mL 1mol•L-1的稀H2SO4溶液,该溶液中含有硫酸的物质的量为:1mol/L×0.1L=0.01mol,设需要需要用量筒量取浓H2SO4(密度为1.84g•mL-1,质量分数为98%)的体积为xmL,由于配制过程中硫酸的量不变,则xmL×1.84g•mL-1×98%=98g/mol×0.01mol,解得:x≈5.4,
故答案为:5.4;
(5)①HCl气体在水溶液中能够导电,属于电解质,但是不能导电;
②Ca(OH)2固体、③KNO3固体在水溶液和熔融状态下能够导电,属于电解质,但是不存在自由移动的阴阳离子,氢氧化钙固体不能导电;
④SO2为非电解质,且不能导电;
⑤Cu为金属单质,既不是电解质也不是非电解质,但能够导电;
⑥氨水为混合物,不是非电解质,但是氨水能够导电;
⑦KNO3溶液为混合物,不属于电解质,但硝酸钾溶液中存在自由移动的离子,能够导电;
⑧石墨为单质,能够导电,不属于电解质;
⑨蔗糖为非电解质,不能导电;
⑩硫酸钡固体为电解质,但是不存在自由移动的离子,不能导电;
根据分析可知,能够导电的为:⑤⑥⑦⑧,属于电解质的为:,
故答案为:⑤⑥⑦⑧;①②③⑩.
点评 本题考查了物质的量的计算、电解质与非电解质的判断的判断,题目难度中等,明确电解质与非电解质的区别为解答关键,注意掌握物质的量与其它物理量之间的转化关系,试题培养了学生的灵活应用能力.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:实验题
 已知热化学方程式H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,
已知热化学方程式H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X一定为电解质 | B. | X可能为NaCl | ||
| C. | X不能是酸类 | D. | X可以是任何化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 480mL | B. | 1000mL | C. | 100mL | D. | 500mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高分子分离膜应用于食品工业中,可用于浓缩天然果汁、乳制品加工、酿酒业等 | |
| B. | 合成高分子材料制成的人工器官一般都受到人体的排斥作用,难以达到生物相容的程度 | |
| C. | 复合材料一般是以一种材料作为基体,另一种材料作为增强剂 | |
| D. | 导电塑料是应用于电子工业的一种新型有机高分子材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分解反应 | B. | 置换反应 | C. | 复分解反应 | D. | 化合反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
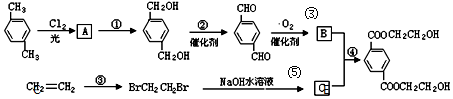
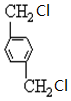 、B、
、B、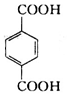 、C.HOCH2CH2OH、
、C.HOCH2CH2OH、 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$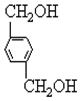 +2NaCl;
+2NaCl; ,反应的化学方程式是
,反应的化学方程式是 +4[Ag(NH3)2]OH$\stackrel{△}{→}$4Ag↓+6NH3↑+
+4[Ag(NH3)2]OH$\stackrel{△}{→}$4Ag↓+6NH3↑+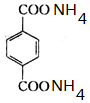 +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com