
【题目】如下图所示,ΔH1=-393.5 kJ·mol-1,ΔH2=-395.4 kJ·mol-1,下列说法正确的是( )

A. 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ
B. 石墨和金刚石的转化是物理变化
C. 金刚石的稳定性强于石墨
D. C(s,石墨)===C(s,金刚石) ΔH=+1.9 kJ·mol-1
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】将CO2气体缓缓地通入到含KOH、Ba(OH)2和KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示。下列关于整个反应进程中的各种描述不正确的是( )

A. o—a段反应的化学方程式是:Ba(OH)2+ CO2===BaCO3↓+ H2O
B. b—c段反应的离子方程式是:2AlO2-+ 3H2O+ CO2===2Al(OH)3↓+ CO32-
C. a—b段与c—d段所发生的反应相同
D. d—e段沉淀的减少是由于碳酸钡固体的消失所致
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列数字代表各元素的原子序数,则各组中相应的元素能形成XY2型离子化合物的是( )
A. 3和8 B. 1和16 C. 12和17 D. 6和16
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液中加入足量Na2O2后仍能大量共存的离子组是( )
A.K+、AlO2-、Cl-、SO42-B.Ca2+、Fe2+、NO3-、HCO3-
C.NH4+、Ba2+、Cl-、NO3-D.Na+、Cl-、CO32-、SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示800℃时A、B、C三种气体物质的浓度随时间变化的情况,t是到达平衡状态的时间。试回答:

(1)该反应的反应物是______。
(2)该反应的化学反应方程式为__________。
(3)若达到平衡状态的时间是2 min,A物质的平均反应速率为(写出简要的计算过程)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 0.1mol/L的NaClO溶液中含有C1O-的数目小于NA
B. 标准状况下,将22.4LC12通入水中,发生反应后,转移的电子数为NA
C. 100g46%的乙醇溶液中,含H-O键的数目为NA
D. 4.6gNa在空气中完全反应生成Na2O、Na2O2,转移0.2NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的用途,说法不正确的是( )
A.水玻璃是建筑行业常用的一种黏合剂
B.碳酸钠是烘制糕点所用发酵剂的主要成分之一
C.硫酸钡医学上用作检查肠胃的内服剂,俗称“钡餐”
D.金属钠可以与钛、锆、铌、钽等氯化物反应置换出对应金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoCl2· 6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、 Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2· 6H2O的工艺流程如下:
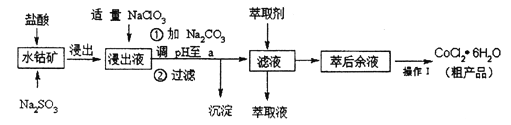
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表(金属离子浓度为0.01 mol/L):
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co (OH) 2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2· 6H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程中主要发生的离子反应方程式:______________。
(2)若不慎向“浸出液”中加过量NaC1O3时,可能会生成的有害气体是_______(填化学式)。
(3)萃取剂对金属离子的萃取率与pH的关系如图,向“滤液”中加入萃取剂的目的是_______,其使用的最佳pH范围是 ________(选填下列字母)。

A. 2.0~2.5 B. 3.0~3.5 C. 4.0~4.5 D. 5.0~5.5
(4) “操作1”是________。制得的CoCl2· 6H2O需减压烘干的原因是__________。
(5)为测定粗产品中CoCl2· 6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2· 6H2O的质量分数大于100%,其原因可能是___________________。(答一条即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中能用平衡移动原理解释的是
A. 使用催化剂可加快氨的合成速率
B. 在FeSO4溶液中,加入铁粉以防止氧化
C. 由H2蒸气、I2蒸气、HI组成的平衡体系加压后颜色变深
D. 硫酸工业生产中,通入过量空气以提高SO2的利用率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com