
【题目】常温下,向![]() 浓度均为
浓度均为![]() 和
和![]() 的混合溶液中滴加
的混合溶液中滴加![]() 的
的![]() ,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积
,测得混合溶液的电阻率(溶液的电阻率越大,导电能力越弱)与加入氨水的体积![]() 的关系如图所示(忽略混合时体积变化),下列说法正确的是( )
的关系如图所示(忽略混合时体积变化),下列说法正确的是( )

A.常温下,![]() 的
的![]() 比同浓度
比同浓度![]() 的
的![]() 大
大
B.![]() 过程中水的电离程度先减小后增大
过程中水的电离程度先减小后增大
C.![]() 点溶液中,
点溶液中,![]()
D.![]() 点时,
点时,![]()
【答案】D
【解析】
电阻率与离子浓度成反比,即a→b过程中溶液的导电性减弱,向混合溶液中加入等物质的量浓度的NH3H2O溶液时,发生反应先后顺序是HX+NH3H2O=NH4X+H2O、NH3H2O+CH3COOH=CH3COONH4+H2O,0-20mL溶液中电阻率增大、导电性减弱,b点最小,原因为溶液体积增大导致b点离子浓度减小,b点溶液中溶质为NH4X、CH3COOH,继续加入NH3H2O溶液,NH3H2O是弱电解质,生成的CH3COONH4是强电解质,导致溶液中离子浓度增大,溶液的电导性增大,c点时醋酸和一水合氨恰好完全反应生成醋酸铵,c点溶液中溶质为NH4X、CH3COONH4,且二者的物质的量相等,d点溶液中溶质为等物质的量浓度的NH4X、CH3COONH4、NH3H2O,据此分析解答。
A.若HX和CH3COOH都是弱酸,则随着NH3H2O的加入,酸碱反应生成盐,溶液导电性将增强、电阻率将减小,但图象上随着NH3H2O的加入溶液电阻率增大、导电性反而减弱,说明原混合溶液中离子浓度更大,即HX为强电解质,常温下,0.1mol/LHX的pH比同浓度CH3COOH的pH小,故A错误;
B.酸或碱都抑制水的电离,滴加NH3H2O溶液的过程:a→c为HX和CH3COOH转化为NH4X、CH3COONH4的过程,溶液的酸性减弱,水的电离程度增大,故B错误;
C.根据分析,c点溶液中溶质为NH4X、CH3COONH4,且二者的物质的量相等,溶液为酸性,即c(H+)>c(OH-),溶液中存在电荷守恒:c(NH4+)+c(H+)=c(OH-)+c(X-)+c(CH3COO-),则c(NH4+)<c(X-)+c(CH3COO-),故C错误;
D.d点溶液中溶质为等物质的量浓度的NH4X、CH3COONH4、NH3H2O,0~40mL时,NH3H2O转化为NH4+,40~60mL时,NH3H2O过量,d点时,溶液体积共为80mL,![]() ,故D正确;
,故D正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉,MnO2,ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料,有关数据如表所示:
溶解度/(g/100g水)
0 | 20 | 40 | 60 | 80 | 100 | |
NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
溶度积常数
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
(1)该电池的正极反应式为______,电池反应的离子方程式为____
(2)维持电流强度为0.5A,电池工作五分钟,理论上消耗Zn_____g。(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过____分离回收;滤渣的主要成分是MnO2、______和______,欲从中得到较纯的MnO2,最简便的方法是_____________,其原理是_______/span>。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为周期表的一部分,其中的编号代表对应的元素。
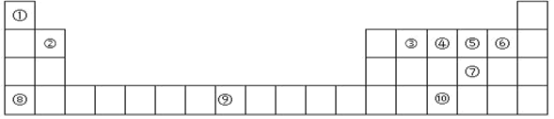
(1)在①~⑩元素的电负性最大的是_____(填元素符号)。
(2)⑨元素有_____种运动状态不同的电子。
(3)⑩的基态原子的价电子排布图为_____。
(4)⑤的氢化物与⑦的氢化物比较稳定的是_____,沸点较高的是_____(填化学式)。
(5)上述所有元素中的基态原子中 4p轨道半充满的是_____(填元素符号),4s轨道半充满的是_____(填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表示正确的是
A. 羟基的电子式:![]()
B. 甘氨酸的结构简式:C2H5NO2
C. AlCl3溶液中Al3+水解的离子方程式:Al3++3H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
D. 粗铜(含Cu及少量Zn、Fe、Ag等)电解精炼时,阳极主要发生反应:Ag-e-=Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验现象和解释或结论都正确的是( )
选项 | 实验操作 | 现象 | 解释或结论 |
A | 取硫酸催化淀粉水解的反应液,滴入少量新制 | 有砖红色沉淀生成 | 葡萄糖具有还原性 |
B |
| 有白色絮状沉淀生成 | 二者水解相互促进生成氢氧化铝沉淀 |
C | 将充满 | 红棕色变深 | 反应 |
D | 向 | 得到红褐色透明液体 | 得到 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是功能性高分子材料的单体,化合物Y是一种抗菌药物,它们的结构简式如下图所示:
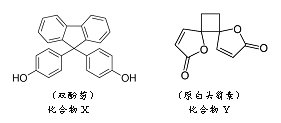
下列说法错误的是
A. X、Y均能与浓Br2水发生反应
B. X分子中四个苯环处于同一平面
C. X、Y分子中手性碳原子数依次为1个、2个
D. 1molX、1molY分别与NaOH反应时,最多消耗NaOH的物质的量均为2mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电能是现代社会应用最广泛的能源之一。
(1)如图所示装置中,Zn是_____极(填“正”或“负”)。
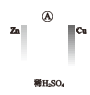
(2)如图所示装置可将______(写化学方程式)反应释放的能量直接转变为电能;能证明产生电能的实验现象是_____。
(3)氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图所示。下列有关氢氧燃料电池的说法,正确的是______。
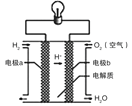
①电极b是正极
②外电路中电子由电极b通过导线流向电极a
③该电池的总反应:2H2+O2=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H[3-亚甲基异苯并呋喃-1(3H)-酮]的一种合成路线如下:
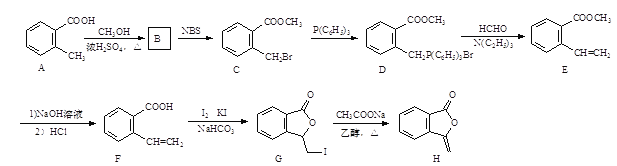
(1)C中所含官能团名称为_________和_________。
(2)G生成H的反应类型是________。
(3)B的分子式为C9H10O2,写出B的结构简式:________。
(4)E的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_________。①分子中含有苯环,能使Br2的CCl4溶液褪色;
②碱性条件水解生成两种产物,酸化后分子中均只有4种不同化学环境的氢,其中之一能与FeCl3溶液发生显色反应。
(5)写出以![]() 、P(C6H5)3及N(C2H5)3为原料制备
、P(C6H5)3及N(C2H5)3为原料制备![]() 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)____。
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1mol·L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数φ(X)随pH的变化如图所示。
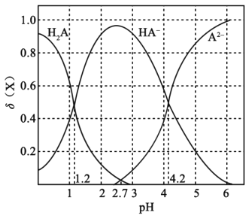
下列叙述错误的是( )
A.pH=1.2时,c(H2A)=c(HA-)
B.lg[K2(H2A)]=-4.2
C.pH=2.7时,c(HA-)>c(H2A)=c(A2-)
D.pH=4.2时,c(HA-)=c(A2-)=c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com