
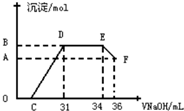
 研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量铁铝合金与一定量很稀的硝酸充分反应,反应过程中无气体放出.往反应结束后的溶液中,逐滴加入2mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.下列选项正确的是( )
研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量铁铝合金与一定量很稀的硝酸充分反应,反应过程中无气体放出.往反应结束后的溶液中,逐滴加入2mol•L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.下列选项正确的是( )| A. | 图中OC段的离子方程式为:NH4++OH-═NH3•H2O | |
| B. | 在DE段的离子方程式为:H++OH-═H2O | |
| C. | B与A的差值为 0.002mol | |
| D. | C点对应的氢氧化钠溶液的体积为7 mL |
分析 铝和铁混合物与一定量很稀HNO3充分反应,被氧化为Al3+、Fe3+,由于反应始终没有气体生成,可以得出不会有氮的氧化物生成,又有硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,可以推测N元素由+5变成了-3价,由图可得硝酸过量,加入氢氧化钠溶液应先与硝酸反应,再生成沉淀,当沉淀完全后,由图知继续加入氢氧化钠溶液,沉淀量不变,可得与NH4+发生了反应,则随着NaOH的滴加,发生的反应依次有:
OC段:H++OH-=H2O,
CD段:Fe3++3OH-=Fe(OH)3↓,Al3++3OH-=Al(OH)3↓,
DE段:NH4++OH-═NH3•H2O,
据此结合图象数据进行解答.
解答 解:铝和铁的混合物与一定量很稀HNO3充分反应,被氧化为Al3+、Fe3+,由于反应始终没有气体生成,可以得出不会有氮的氧化物生成,又有硝酸的浓度越稀,对应还原产物中氮元素的化合价越低,可以推测N元素由+5变成了-3价,由图可得硝酸过量,加入氢氧化钠溶液应先与硝酸反应,再生成沉淀,当沉淀完全后,由图知继续加入氢氧化钠溶液,沉淀量不变,可得与NH4+发生了反应,则随着NaOH的滴加,发生的反应依次有:OC段:H++OH-=H2O,CD段:Fe3++3OH-=Fe(OH)3↓,Al3++3OH-=Al(OH)3↓,DE段:NH4++OH-═NH3•H2O,
A.OC段没有沉淀生成,说明稀硝酸过量,加入的氢氧化钠与稀硝酸反应生成硝酸钠和水,反应的离子方程式为:H++OH-=H2O,故A错误;
B.DE段生成的沉淀的物质的量不变,说明铵根离子与氢氧根离子反应,反应的离子方程式为:DE段:NH4++OH-═NH3•H2O,故B错误;
C.氢氧化镁不与氢氧化钠反应,则B与A的差值为氢氧化铝的物质的量,EF段消耗的氢氧化钠为:n(NaOH)=2mol/L×2×10-3L=0.004mol,根据反应Al(OH)3+NaOH=NaAlO2+2H2O可知氢氧化铝的物质的量为0.004mol,则B与A的差值为 0.004mol,故C错误;
D.DE段是NH4NO3和NaOH反应,根据反应NH4NO3~NaOH可知:n(NH4NO3)=n(NaOH)=(34-31)×10-3L×2mol/L=0.006mol,
设铁有xmol,铝离子的物质的量为0.004mol,NH4+有0.006mol,根据电子守恒可得:3x+0.004×3=0.006×8,解得x=0.012mol,
所以铁离子有0.012mol,根据原子守恒知,铁的物质的量是0.012mol;
滴加NaOH体积为31mL时,发生反应为:H++OH-=H2O、Fe3++3OH-=Fe(OH)3↓、Al3++3OH-=Al(OH)3↓,
所以C点氢氧化钠溶液的体积为:31mL-$\frac{0.012mol×3+0.004mol×3}{2mol/L}$×103ml/L=7mL,故D正确;
故选D.
点评 本题考查了氧化还原反应的计算,题目难度中等,明确图象曲线变化对应反应原理为解答关键,注意掌握守恒思想在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 利用电池外壳的金属材料 | |
| B. | 防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 | |
| C. | 不使电池中渗泄的电解液腐蚀其他物品 | |
| D. | 回收其中石墨电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH | CH3OCH3 | H2O | ||
| Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 207 | 0.20 | 0.090 | 0.090 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
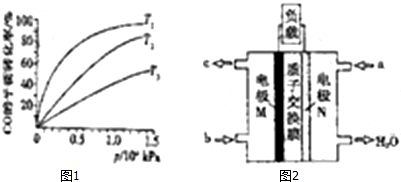
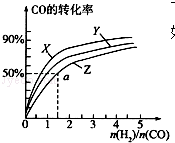 甲醇是重要的燃料,有广阔的应用前景:工业上一般以CO和为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)═CH3OH(g)△H1=-116kJ•mol-1
甲醇是重要的燃料,有广阔的应用前景:工业上一般以CO和为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)═CH3OH(g)△H1=-116kJ•mol-1查看答案和解析>>
科目:高中化学 来源: 题型:解答题
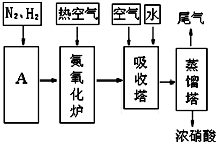
 CO+3H2.
CO+3H2.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 3:1 | B. | 4:1 | C. | 3:2 | D. | 7:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,1mol氦气含有的原子数为NA | |
| B. | 标准状况下,5.6L四氯化碳含有的分子数为0.25NA | |
| C. | 标准状况下,32gSO2的体积约为22.4L | |
| D. | 物质的量浓度为1mol•L-1的K2SO4溶液中,含2NA个K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com