
| A. | ③④ | B. | ②③④ | C. | ②③ | D. | 全部 |
分析 中学常见的既能与酸反应又能与碱反应的物质主要有:①两性物质:Al2O3、Al(OH)3、氨基酸、蛋白质等;②多元弱酸的酸式盐:NaHCO3、KHS、KHSO3、NaH2PO4等;③弱酸的铵盐及其酸式盐:(NH4)2S、NH4HS、(NH4)2CO3、NH4HCO3、CH3COONH4等;④某些具有两性的金属:Zn、Al等.
解答 解:①Na2CO3能与盐酸反应生成氯化钠、二氧化碳与水,不能与氢氧化钠反应,故①不符合;
②Al能与盐酸反应生成氯化铝与氢气,与氢氧化钠溶液反应生成偏铝酸钠与羧酸,故②符合;
③Al2O3 是两性氧化物,既能与盐酸反应生成铝盐(Al3+),又能与氢氧化钠反应生偏铝酸盐(AlO2-),故③符合;
④Al(OH)3 是两性氢氧化物,既能与盐酸反应生成铝盐(Al3+),又能与氢氧化钠反应生偏铝酸盐(AlO2-),故④符合;
故选B.
点评 本题考查元素化合物的性质,题目难度不大,旨在考查学生对知识的理解识记与知识归纳,注意基础知识的积累,注意归纳总结既能与酸又能与碱反应的物质.


科目:高中化学 来源: 题型:解答题
 烟气的脱硫(除SO2)和脱硝(除NOx)都是环境科学研究的热点.可以通过氧化还原反应或酸碱反应进行脱硫和脱硝.
烟气的脱硫(除SO2)和脱硝(除NOx)都是环境科学研究的热点.可以通过氧化还原反应或酸碱反应进行脱硫和脱硝.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L乙醇所含的分子数为NA | |
| B. | 1mol/LCaCl2溶液中含有的氯离子数目为2NA | |
| C. | 1 mol金属钠在足量氧气中完全燃烧转移的电子数为2NA | |
| D. | 28g N2中含有的原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 价电子排布为4s24p2的元素位于第四周期第ⅤA族,是P区元素 | |
| B. | 1,2-二甲苯核磁共振氢谱中有三组峰,且氢原子数之比为3:1:1 | |
| C. | 钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态 | |
| D. | 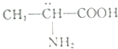 分子属于手性分子 分子属于手性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. +2C2H5OH$→_{△}^{浓硫酸}$
+2C2H5OH$→_{△}^{浓硫酸}$ +2H2O.
+2H2O. 与足量NaOH水溶液反应的化学方程式为
与足量NaOH水溶液反应的化学方程式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲、乙、丙是三种常见单质,A、B、C是常见化合物,B在常温下为液态.在一定条件下上述物质之间的关系如图.
甲、乙、丙是三种常见单质,A、B、C是常见化合物,B在常温下为液态.在一定条件下上述物质之间的关系如图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com