

 CO2(g)+H2(g),该反应的△H________0(选填:“>”、“<”、“=”);在900K时,该反应平衡常数的对数值(lgK)=_____________.
CO2(g)+H2(g),该反应的△H________0(选填:“>”、“<”、“=”);在900K时,该反应平衡常数的对数值(lgK)=_____________.
 Cu2++H2↑
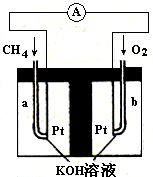
Cu2++H2↑  CO2(g)+H2(g),它的平衡常数为:K="{" C(CO2)·C(H2)} /{ C(CO) ·C(H2O)}.="K2/K1." K越大,lgK就越大。升高温度K减小,说明升高温度化学平衡向逆反应方向移动。根据化学平衡移动原理:升高温度,化学平衡向吸热反应方向移动。逆反应是吸热反应。所以正反应为放热反应。所以△H<0.在900K时,该反应平衡常数的对数值lgK ="lgK2/K1=lgK2-lgK1=-0.03+0.39=0.36." (2)由题意可写出CO、CH3OH燃烧的热化学方程式①CO(g)+(1/2)O2(g)=CO2(g) △H=-283.0KJ/mol;②CH3OH(l)+(3/2)O2(g)=CO2(g)+2H2O.②-①得:CH3OH(l)+O2(g)=CO(g)+2H2O(l);△H=-443.5KJ/mol。(3)根据题意可得反应的化学方程式:3CO+3H2 =(CH3)2O+CO2或者2CO+4H2 =(CH3)2O+ H2O。(4)在燃料电池中,通入燃料的电极作负极,通入氧气的电极作正极。a电极及负极上发生反应的电极反应式是:(CH3)2O-12e-+3H2O=2CO2+12H+。(5)在电解池中观察到装置中电解质溶液颜色由无色变为蓝色,并逐渐加深。说明Cu失去了电子。Cu电极作阳极。二甲醚燃料电池中b电极(即正极)相连。通电时发生反应的总的离子反应方程式为:Cu+2H+
CO2(g)+H2(g),它的平衡常数为:K="{" C(CO2)·C(H2)} /{ C(CO) ·C(H2O)}.="K2/K1." K越大,lgK就越大。升高温度K减小,说明升高温度化学平衡向逆反应方向移动。根据化学平衡移动原理:升高温度,化学平衡向吸热反应方向移动。逆反应是吸热反应。所以正反应为放热反应。所以△H<0.在900K时,该反应平衡常数的对数值lgK ="lgK2/K1=lgK2-lgK1=-0.03+0.39=0.36." (2)由题意可写出CO、CH3OH燃烧的热化学方程式①CO(g)+(1/2)O2(g)=CO2(g) △H=-283.0KJ/mol;②CH3OH(l)+(3/2)O2(g)=CO2(g)+2H2O.②-①得:CH3OH(l)+O2(g)=CO(g)+2H2O(l);△H=-443.5KJ/mol。(3)根据题意可得反应的化学方程式:3CO+3H2 =(CH3)2O+CO2或者2CO+4H2 =(CH3)2O+ H2O。(4)在燃料电池中,通入燃料的电极作负极,通入氧气的电极作正极。a电极及负极上发生反应的电极反应式是:(CH3)2O-12e-+3H2O=2CO2+12H+。(5)在电解池中观察到装置中电解质溶液颜色由无色变为蓝色,并逐渐加深。说明Cu失去了电子。Cu电极作阳极。二甲醚燃料电池中b电极(即正极)相连。通电时发生反应的总的离子反应方程式为:Cu+2H+ Cu2++H2↑。
Cu2++H2↑。

科目:高中化学 来源:不详 题型:单选题
A.H2O(g)=H2(g)+ O2(g)ΔH=242 kJ·mol-1 O2(g)ΔH=242 kJ·mol-1 |
| B.2H2(g)+O2(g)=2H2O(l)ΔH=-484 kJ·mol-1 |
C.H2(g)+ O2(g)=H2O(g)ΔH=242 kJ·mol-1 O2(g)=H2O(g)ΔH=242 kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(g)ΔH=484 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NO2(g);△H=" +57.0" kJ·mol-1,NO2和N2O4的浓度如图甲所示。NO2和N2O4的消耗速率与其浓度的关系如乙图所示,
2NO2(g);△H=" +57.0" kJ·mol-1,NO2和N2O4的浓度如图甲所示。NO2和N2O4的消耗速率与其浓度的关系如乙图所示,
 2NO2(g) △H=" +57.0" kJ·mol-1
2NO2(g) △H=" +57.0" kJ·mol-1 查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
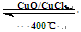 2Cl2(g)+2H2O(g) ΔH=" —115.6" kJ/mol
2Cl2(g)+2H2O(g) ΔH=" —115.6" kJ/mol 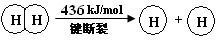

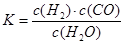 ,它所对应的化学方程式为:
,它所对应的化学方程式为:  2NH3(g) △H<0 的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正 v(N2)逆(填:>、<、=、不能确定)(1分)
2NH3(g) △H<0 的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正 v(N2)逆(填:>、<、=、不能确定)(1分) 2C(g) + D(s) ΔH,其化学平衡常数K与温度t的关系如下表:
2C(g) + D(s) ΔH,其化学平衡常数K与温度t的关系如下表:| t/K | 300 | 400 | 500 | … |
| K/(mol·L—1)2 | 4×106 | 8×107 | K1 | … |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3的平衡常数见下表。
2SO3的平衡常数见下表。| 温度(℃) | 527 | 758 | 927 |
| 平衡常数 | 784 | 1.0 | 0.04 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 CH3OH(g) ΔH1
CH3OH(g) ΔH1 CH3OH(g)+ H2O(g) ΔH2
CH3OH(g)+ H2O(g) ΔH2
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g) ΔH=-196.6 kJ·mol-1反应过程的能量变化示意图。
2SO3(g) ΔH=-196.6 kJ·mol-1反应过程的能量变化示意图。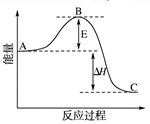
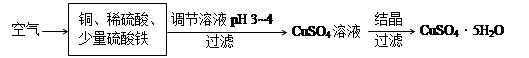
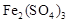 起催化作用,使反应按以下两步完成:
起催化作用,使反应按以下两步完成:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如下:
CO(NH2)2(l)+H2O(l),该反应的平衡常数和温度关系如下:| T / ℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
 ?2NH3(g) ΔH2=-92.4 kJ·mol-1
?2NH3(g) ΔH2=-92.4 kJ·mol-1查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com