
| A. | H2O2溶液中加入MnO2可制得O2,产生2.24L(标况)O2,转移0.4NA个电子 | |
| B. | SO2和CO2都属于酸性氧化物,Na2O和A12O3都属于碱性氧化物 | |
| C. | 在氯化铵水溶液中,既存在水解平衡,又存在电离平衡 | |
| D. | O2在放电的条件下生成O3属于化学变化,电解质溶液导电属于物理变化 |
分析 A.双氧水中氧元素的化合价为-1价,标况下2.24L氧气的物质的量为0.1mol,转移了0.2mol电子;
B.氧化铝为两性氧化物,不属于碱性氧化物;
C.硫化铵溶液中存在铵根离子的水解平衡,还存在水的电离平衡;
D.电解质溶液的导电是电解,过程有新物质生成,属于化学变化.
解答 解:A.标况下2.24L氧气的物质的量为:$\frac{2.24L}{22.4L/mol}$=0.1mol,双氧水中氧元素的化合价为-1价,则生成0.1mol氧气转移了0.2mol电子,转移0.2NA个电子,故A错误;
B.SO2和CO2都能够与碱溶液反应生成盐和水,属于酸性氧化物,Na2O能够与酸反应生成盐和水,属于碱性氧化物,而A12O3能够与酸和强碱溶液反应,属于两性氧化物,故B错误;
C.在氯化铵水溶液中,既存在铵根离子的水解平衡,又存在水的电离平衡,故C正确;
D.氧气转化成臭氧反应中有新物质生成,属于化学变化,而电解质溶液的导电是电解过程,有新物质生成,属于化学变化,故D错误;
故选C.
点评 本题考查了阿伏伽德罗常数的应用、化学变化与物理变化的判断、酸性、碱性氧化物的判断等知识,试题知识点较多,充分考查学生灵活应用基础知识的能力,注意溶液导电过程为化学变化,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | CO32-+2H+═H2O+CO2↑ | B. | CO32-+H+═H2O+CO2↑ | ||
| C. | CO32-+2HCl═2Cl-+H2O+CO2↑ | D. | Na2CO3+2H+═2Na++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸和NaOH溶液混合 | B. | 氯化氢溶于水 | ||
| C. | 溴化氢气体与氨气相遇反应 | D. | 锌和稀硫酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol苯分子中含有碳碳双键数为3NA | |
| B. | 1mol氯化氢分子中含H+离子数为NA | |
| C. | 16 gCH4与18g NH4+ 所含质子数均为NA | |
| D. | 4.6 g钠与足量盐酸完全反应失去电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 空气是一种宝贵的资源 | |
| B. | 空气中氮气的质量分数为78% | |
| C. | 氧气易溶于水,供给水生生物呼吸 | |
| D. | 汽车尾气随意排放,与雾霾形成无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F分别是氧化铁、二氧化碳、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液中的一种;已知C在日常生活中常用来灭火.六种物质之间有如图所示的反应关系,图中相连的两圆表示相应物质间能发生反应.回答下列问题:
A、B、C、D、E、F分别是氧化铁、二氧化碳、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液中的一种;已知C在日常生活中常用来灭火.六种物质之间有如图所示的反应关系,图中相连的两圆表示相应物质间能发生反应.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
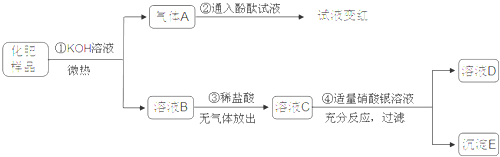
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2L SO3含有的分子数少于0.5NA | |
| B. | 1mol•L-1的Ca(ClO)2溶液中含ClO-数目为2NA | |
| C. | 标准状况下,2.24L四氯化碳中“C-Cl”键为0.4NA | |
| D. | 1molNa被完全氧化生成Na2O2,失去2NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com