
| A�� | ������ˮϴ���ձ���������2��3�Σ�ÿ��ϴ�Ӻ����Һ��ע������ƿ�� | |
| B�� | �ѳ�����NaOH�������ʢ����������ˮ���ձ��У��ܽ����������Һת�Ƶ�����ƿ�� | |
| C�� | ��������ƽ�����������ϸ���һ�Ŵ�Сһ����ֽ��Ȼ��NaOH�������ֽ�Ͻ��г��� | |
| D�� | ���Ų�����������ƿ�м�������ˮ��ֱ����Һ��Һ��ǡ����̶����� |
���� A���ձ���������ϴ�ӣ�����������ʣ�
B��Ӧ��ȴ��ת�ƣ�
C��NaOH�׳��⣬���и�ʴ�ԣ�
D������ʱ��ˮ���̶���1��2cm�������ý�ͷ�ιܵμӣ�
��� �⣺A���ձ���������ϴ�ӣ�����������ʣ���������ˮϴ���ձ���������2��3�Σ�ÿ��ϴ�Ӻ����Һ��ע������ƿ�У���A��ȷ��
B��Ӧ��ȴ��ת�ƣ������ܽ����������Һת�Ƶ�����ƿ�У���B����
C��NaOH�׳��⣬���и�ʴ�ԣ���Ӧ��NaOH��С�ձ��г�������C����
D������ʱ��ˮ���̶���1��2cm�������ý�ͷ�ιܵμӣ�����Һ��Һ��ǡ����̶����У���D����
��ѡA��
���� ���⿼����Һ�����ƣ�Ϊ��Ƶ���㣬����������Һ�IJ�����������ʵ�鼼��Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬ע��ʵ�������������Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��CO��g��+H2S��g��?COS��g��+H2��g���ﵽƽ��������¶ȣ�H2SŨ�����ӣ������÷�Ӧ�����ȷ�Ӧ | |
| B�� | ��CO��g��+H2S��g��?COS��g��+H2��g���ﵽƽ���ͨ��CO������Ӧ���������� | |
| C�� | һ�������·�ӦN2+3H2?2NH3�ﵽƽ��ʱ��3v����H2��=2v�棨NH3�� | |
| D�� | ���ڷ�ӦCO��g��+H2O��g��?CO2��g��+H2��g����H��0��ֻ�ı�ѹǿ��ƽ�ⲻ�����ƶ�����Ӧ�ų����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | t1sʱ��Ӧ��A��ת����Ϊ60% | |
| B�� | ��t1����t1+10��sʱ��v��A��=v��B��=0 | |
| C�� | �÷�Ӧ�Ļ�ѧ����ʽΪ3A+B?2C | |
| D�� | 0��t1s��A�ķ�Ӧ����Ϊv��A��=$\frac{0.2}{{t}_{1}}$mol/��L•s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������FeCl3��Һ�μ�����ˮ��ֱ�Ӿ����Ƶ�Fe��OH��3���� | |
| B�� | ����������������ɢϵ�ı��������ǽ������ӵ�ֱ����С | |
| C�� | �ù��˵ķ������Է�����ᴿ���� | |
| D�� | ���Ĺ����з����˽���ĵ�Ӿ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ӿ��������� | B�� | �����ǻ�ԭ�� | ||
| C�� | ��������������Ӧ | D�� | �����ԣ�Cl2��Br2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
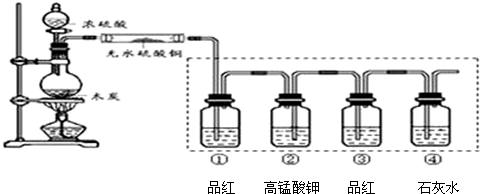
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
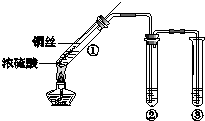 ijС��ͬѧ̽��Ũ���ἰ�䲿�ַ�Ӧ����Ļ�ѧ���ʣ�װ����ͼ��ʾ���г�װ����ȥ����
ijС��ͬѧ̽��Ũ���ἰ�䲿�ַ�Ӧ����Ļ�ѧ���ʣ�װ����ͼ��ʾ���г�װ����ȥ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��� | ���� | ���� | ���� | ���� |
| ��װ�� |  |  |  | 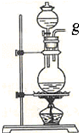 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʱ��/s | 0 | 50 | 150 | 250 | 350 |
| n��PCl3��/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
| A�� | ��Ӧ��ǰ50s��ƽ����Ӧ����Ϊv��PCl3��=0.0064 mol/��L•s�� | |
| B�� | �����������������䣬�����¶ȣ�ƽ��ʱc��PCl3��=0.11 mol/L����Ӧ�ġ�H��0 | |
| C�� | ��ͬ�¶��£���ʼʱ��������г���4.0 mol PCl3��4.0 mol Cl2���ﵽƽ��ʱ��PCl3��ת����С��80% | |
| D�� | ��ͬ�¶��£���ʼʱ��������г���2.0 mol PCl5��0.40 mol PCl3��0.40 mol Cl2���ﵽƽ��ǰv��������v���棩 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com