
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C | Cl-Cl |
| 键能/kJ•mol-1 | 460 | 360 | 436 | 431 | 176 | 347 | 243 |
| A. | 表中最稳定的共价键是Si-Si | |
| B. | Cl2(g)→2 Cl(g):△H=-243 kJ•mol | |
| C. | H2 (g)+Cl2(g)=2HCl(g):△H=-183 kJ•mol | |
| D. | 根据表中数据能计算出SiCl4(g)+2 H2(g)═Si(s)+4 HCl(1)的△H |
分析 A.键能越大形成的化学键越稳定;
B.氯气变化为氯原子吸热等于氯气中断裂化学键需要的能量;
C.依据键能计算反应焓变=反应物键能总和-生成物键能总和计算判断;
D.由于HCl(g)=HCl(l)的△H未告知,无法计算,据此解答即可.
解答 解:A.键能越大形成的化学键越稳定,表中键能最大的是Si-O,最稳定的共价键是Si-O键,故A错误;
B.氯气变化为氯原子吸热等于氯气中断裂化学键需要的能量,Cl2(g)→2Cl (g)?△H=+243 kJ•mol-1 ,故B错误;
C.依据键能计算反应焓变=反应物键能总和-生成物键能总和计算判断,△H=436kJ/mol+243kJ/mol-2×431k/mol=-183kJ/mol,H2(g)+Cl2(g)=2HCl(g)?△H=-183kJ•mol-1,故C正确;
D.HCl(g)=HCl(l)的△H未告知,故无法计算SiCl4(g)+2 H2(g)=Si(s)+4 HCl(1)的△H,故D错误;
故选C.
点评 本题主要考查的是反应热与焓变,利用键能计算反应热时利用公式-断开旧化学键吸收的能量-生成新化学键放出的能量,难度不大,注意物质的状态.


科目:高中化学 来源: 题型:选择题
| A. | Ba2+、Al3+、NO3-、SO42- | B. | Na+、CI-、Ca2+、NO3- | ||
| C. | OH-、NH4+、Na+、SO42- | D. | Fe3+、K+、Cl-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
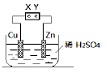
| A. | 直接连接X、Y,则该装置可将电能转变为化学能 | |
| B. | 直接连接X、Y,生成2.24LH2时一定转移0.2mole- | |
| C. | 将X、Y与直流电源相连,一段时间后,Zn片质量一定减少 | |
| D. | 将X、Y与直流电源相连,则该装置可能发生反应:Cu+H2SO4$\frac{\underline{\;通电\;}}{\;}$CuSO4+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol/L | B. | 10mol/L | C. | 0.01mol/L | D. | 0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
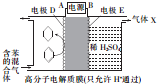
| A. | 电子流向:D→A,B→E | |
| B. | 气体X为O2 | |
| C. | 电极D为惰性电极,E为活泼电极 | |
| D. | 电极D的电极反应式为C6H6+6H++6e-═C6H12 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的$\frac{2}{3}$ |
| Z | 第三周期原子半径最小的金属 |
| A. | 气态氢化物的热稳定性:X>W | |
| B. | 最高价氧化物对应水化物的酸性:Y>X | |
| C. | 离子半径:Z>W | |
| D. | X在自然界中以游离态和化合态形式存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称取12.5g胆矾(CuSO4•5H2O),配成500mL溶液 | |
| B. | 称取12.5g胆矾(CuSO4•5H2O),加入500mL水配成溶液 | |
| C. | 称取7.68g无水硫酸铜粉末,加入480mL水配成溶液 | |
| D. | 称取8.0g无水硫酸铜粉末,加入500mL水配成溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ⑧ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
| 4 | ⑨ |
 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com