
【题目】下列不能用勒夏特列原理解释的是
A. 开启汽水瓶后,瓶中马上泛起大量泡沫
B. Cl2(HCl)要除去其中的HCl,将其通过饱和食盐水
C. 在N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0 中,反应条件是高温、高压催化剂
2NH3(g) ΔH<0 中,反应条件是高温、高压催化剂
D. SO2催化氧化成SO3的反应,往往需要使用过量的空气
【答案】C
【解析】
A. 在汽水中存在可逆反应:CO2+H2O![]() H2CO3,开启汽水瓶后,瓶中马上泛起大量泡沫,是压强对其影响导致的,能用勒夏特列原理解释,故A不选;
H2CO3,开启汽水瓶后,瓶中马上泛起大量泡沫,是压强对其影响导致的,能用勒夏特列原理解释,故A不选;
B. Cl2+H2O![]() H++Cl-+HClO,饱和食盐水中氯离子浓度较大,使Cl2+H2O
H++Cl-+HClO,饱和食盐水中氯离子浓度较大,使Cl2+H2O![]() H++Cl-+HClO平衡逆向移动,导致氯气在饱和食盐水中溶解度降低,能用勒夏特列原理解释,故B不选;
H++Cl-+HClO平衡逆向移动,导致氯气在饱和食盐水中溶解度降低,能用勒夏特列原理解释,故B不选;
C. 合成氨反应为放热反应,升高温度不利于平衡向正方向移动,高温主要考虑的是催化剂的活性和反应速率,与平衡移动无关,不能用勒夏特列原理解释,故C选;
D. SO2催化氧化成SO3的反应,方程式为2SO2+O2![]() 2SO3,使用过量的氧气,平衡向正反应方向移动,能用勒夏特列原理解释,故D不选,答案选C。
2SO3,使用过量的氧气,平衡向正反应方向移动,能用勒夏特列原理解释,故D不选,答案选C。


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,下列有关离子浓度关系的比较,正确的是
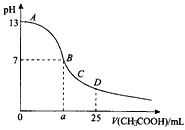
A. A、B之间任意一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B. B点,a>12.5,且有c(Na+)=c(CH3COO-)=c(OH-)=c(H+)
C. C点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D. D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fenton法常用于处理含难降解有机物的工业废水,往调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p﹣CP,控制p﹣CP的初始浓度相同,恒定实验温度在298K或313K进行实验。实验测得p﹣CP的浓度随时间变化的关系如图所示,下列说法不正确的是( )
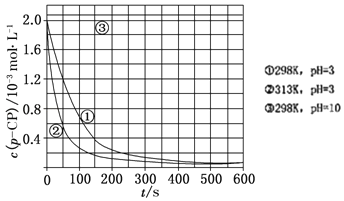
A.由①可得,降解反应在50~150s内的反应速率:v(pCP)=8.0×10﹣6molL﹣1s﹣1
B.升高温度,有利于加快降解反应速率,但温度过高反应速率又会变慢
C.③目的为探究溶液的pH对降解反应速率的影响
D.298K下,有机物p﹣CP降解速率pH=10时比pH=3快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为周期表的一部分,表中所列的字母分别代表一种化学元素。回答下列问题:
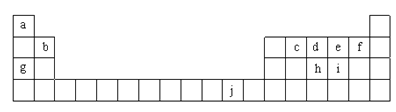
(1)f的基态原子核外电子排布式______。
(2)在c2a4分子中,c为______杂化,c与c间存在的共价键类型有______两种。
(3)ci2与ce2比较,沸点较高的是______(写分子式),其原因是_________________。
(4)将氨水滴入到j的硫酸盐溶液中,先产生蓝色沉淀,然后沉淀逐渐溶解并得到深蓝色溶液。深蓝色溶液是由于存在______(写结构式),其中配体是_____。
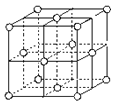
(5)j的金属晶体的晶胞如图所示,则一个晶胞中每个j原子周围与它最接近且距离相等的j共有的个数是______个,已知该元素的相对原子质量为64,单质晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA,试求铜的金属半径为__________ pm(用含NA、ρ的表达式表达)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】资料显示:氨气可在纯氧中安静燃烧![]() 某校化学小组学生设计如下装置
某校化学小组学生设计如下装置![]() 图中铁夹等夹持装置已略去
图中铁夹等夹持装置已略去![]() 进行氨气与氧气在不同条件下反应的实验;
进行氨气与氧气在不同条件下反应的实验;

(1)氨气极易溶于水,其水溶液叫做氨水,显______性,能使石蕊试液变______;其原因为____________![]() 用化学方程式和电离方程式表示
用化学方程式和电离方程式表示![]()
(2)图甲是实验室制取纯净、干燥的氨气的装置图,写出大试管内发生反应的化学方程式![]() 采用实验室常用药品制氨气
采用实验室常用药品制氨气![]() :______,A中所加药品为______,所起作用为______.
:______,A中所加药品为______,所起作用为______.
(3)将产生的氨气与过量的氧气通到装置乙中,用酒精喷灯加热后,试管内气体为______色,氨催化氧化的化学方程式是______
(4)将过量的氧气与甲产生的氨气分别从a、b两管进气口通入到装置丙中,并在b管上端点燃氨气,其氧化产物为空气的主要成分之一;
![]() 两气体通入的先后顺序是______;
两气体通入的先后顺序是______;![]() 氨气燃烧的化学方程式是______.
氨气燃烧的化学方程式是______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图曲线表示其他条件一定时,反应2M(g)+N(g)![]() 2R(g) ΔH<0,达到平衡时N的体积分数与温度的关系曲线,图中标有a、b、c、d四点,其中v正<v逆的点是
2R(g) ΔH<0,达到平衡时N的体积分数与温度的关系曲线,图中标有a、b、c、d四点,其中v正<v逆的点是
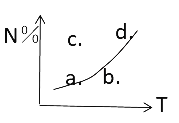
A. a点 B. b点
C. c点 D. d点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化钠和过氧化钠的叙述中不正确的是
A.Na2O2是淡黄色固体,Na2O是白色固体,阴阳离子个数比均为1:2
B.Na2O2和Na2O均为碱性氧化物,都能与水反应生成NaOH
C.Na2O和Na2O2均能与CO2发生反应,都有Na2CO3生成
D.2gH2充分燃烧后产物被Na2O2完全吸收,Na2O2固体增重2g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有Na+、Ba2+、Cu2+、CO32-、Cl-、Mg2+中的一种或几种离子。
①向此溶液中滴加足量稀盐酸无明显现象。
②取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。
③取②的上层清液并加入足量的NaOH溶液,有白色沉淀产生。
(1)原溶液中一定含有的离子是________,一定不含有的离子是________,不能确定是否含有的离子是________。
(2)②中反应的离子方程式为___________________。
(3)若另取10mL①的溶液于锥形瓶中,然后向此溶液中逐滴加入NaOH溶液(如图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示。
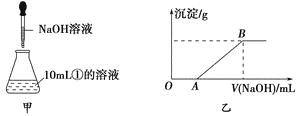
①OA段反应的离子方程式为_____________________。
②AB段反应的离子方程式为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五氧化二钒(V2O5,摩尔质量为182g·mol-1)可作化学工业中的催化剂,广泛用于冶金、化工等行业。V2O5是一种橙黄色片状晶体,微溶于水,不溶于乙醇,具有强氧化性,属于两性氧化物。某研究小组将从某粗钒(主要含有V2O5,还有少量Al2O3、Fe2O3)中提取V2O5。实验方案设计如下:
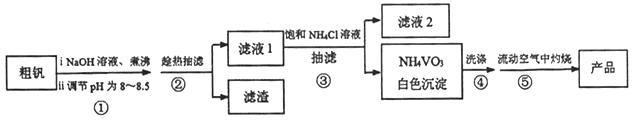
已知:NH4VO3是白色粉末,微溶于冷水,可溶于热水,不溶于乙醇、醚。
2NH4VO3![]() V2O5+2NH3↑+H2O
V2O5+2NH3↑+H2O
请回答:
(1)第①步操作的实验装置如右图所示,虚线框中最为合适的仪器是________。(填编号)
![]()
![]()
![]()
![]()
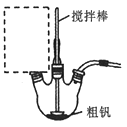
(2)调节pH为8~8.5的目的________。
(3)第④步洗涤操作时,可选用的洗涤剂_________。(填编号)
A.冷水 B.热水 C.乙醇 D.1%NH4Cl溶液
(4)第⑤步操作时,需在流动空气中灼烧的可能原因________。
(5)硫酸工业中,SO2转化为SO3的催化剂就选用V2O5,催化过程经两步完成,将其补充完整:________(用化学方程式表示),4VO2+O2=2V2O5。
(6)将0.253g产品溶于强碱溶液中,加热煮沸,调节pH为8~8.5,向反应后的溶液中加入硫酸酸化的KI溶液(过量),溶液中含有V3+,滴加指示剂,用0.250mol·L-1Na2S2O3溶液滴定,达到终点消耗Na2S2O3标准溶液20.00mL,则该产品的纯度为________。(已知:I2+2Na2S2O3=Na2S4O6+2NaI)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com