
钾水玻璃以其优异的性能广泛用于防腐、铸造、油田、钻井或各种高档涂料中。钾水玻璃中硅含量的测定可以采用氟硅酸钾容量法,其步骤为:
①称取试样溶解在含有过量的氟离子和钾离子的强酸溶液中,硅能与氟离子、钾离子作用生成氟硅酸钾(K2SiF6)沉淀;
②沉淀分离后于热水中水解,生成HF、H2SiO3、KF;
③过滤除去硅酸沉淀,用氢氧化钠标准溶液滴定滤液。
(1)上述步骤②中的水解反应方程式为 ▲ ;
步骤③中反应的离子方程式为: ▲ 。
(2)在步骤③中,若滴定前未用氢氧化钠标准溶液润洗滴定管,则测得的硅元素含量将
▲ (填“偏高”、或“偏低”或“不变”)。
(3)若每次称取试样的质量为1.00g,重复滴定四次,消耗1.00 mol·L-1氢氧化钠标准溶液的体积为分别为16.80mL、19.90mL、20.00mL、20.10mL,试计算该试样中硅元素的质量分数(以二氧化硅计),写出计算过程。 ▲
科目:高中化学 来源: 题型:
 下列实验问题的处理方法中,正确的是
下列实验问题的处理方法中,正确的是
|
| A. | 实验中不慎打破温度计,可用吹风机加快水银的蒸发 |
|
| B. | 在气体发生装置上直接点燃甲烷气体时,必须先检验甲烷的纯度 |
|
| C. | 实验结束后,将废液倒入下水道排出实验室,以免污染实验室 |
|
| D. | 燃着的酒精灯不慎碰翻失火,应立即用水扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:
50 g物质的量浓度为c1的浓H2SO4质量分数w1,与V mL水混合,得到物质的量浓度为c2的稀H2SO4质量分数为w2以下填“<”“>”或“=”
(1)若w1=2w2,则c1________2c2,V________50 mL。
(2)若c1=2c2,则w1________2w2,V________50 mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列相关反应的离子方程式书写正确的是 ( )
A.用小苏打治疗胃酸过多:CO32- + 2H+ = CO2↑ + H2O
B.稀硝酸中加入过量的铁粉:Fe + 4H+ + NO3-=Fe2+ + NO↑ + 2H2O
C.Ba(HCO3)2溶液中加入过量的NaOH溶液:2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32-
D.NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:
Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
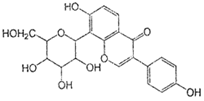
葛根素具有降血压等作用,其结构简式如下图,下列有关说法正确的是( )
A.该物质在一定条件下能发生消去反应、加成反应、取代反应
B.葛根素的分子式为C21H22O9
C.该物质一个分子中含有5个手性碳原子
D.一定条件下1 mol 该物质与H2反应最多能消耗7 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与日常生活密切相关,下列说法正确的是( )
A. 碘酒只是指碘单质的乙醇溶液
B. 纯水不易导电,但属于电解质
C. 质量分数:医用酒精>生理盐水>食醋
D. 明矾可用于水的消毒、杀菌
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,反应后固体物质增重的是( )
|
| A. | 氢气通过灼热的CuO粉末 | B. | 二氧化碳通过Na2O2粉末 |
|
| C. | 铝与Fe2O3发生铝热反应 | D. | 将锌粒投入Cu(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室从含碘废液(除H2O外,还含有CCl4、I2、I﹣)中回收碘,其实验过程如图1:
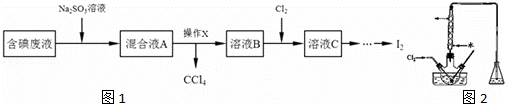
(1)向含碘废液中加入稍过量的Na2SO3溶液时发生的离子方程式为 ;该操作的目的是 .
(2)操作X应在 (填写仪器名称图2)中进行,简述得到溶液B的过程:将混合溶液静置后,
(3)在三颈瓶中将溶液B用盐酸调至pH约为2,缓慢通入Cl2,在40˚C左右反应(实验装置如右图所示).实验控制在较低温度下进行的原因是 ;锥形瓶里盛放的溶液为 (填溶质的化学式).
(4)某含碘废水(pH约为4)中一定存在I2,可能存在I﹣或IO3﹣.可以使用 (填溶质的化学式,下同)溶液检验可能存在的I﹣或 溶液检验可能存在的IO3﹣.在检验该含碘废水中是否含有I﹣或IO3﹣前必需要进行的操作是 (填序号).
a.取适量含碘废水用CCl4多次萃取、分液
b.用NaOH溶液将溶液调节到中性
c.向溶液中滴入少量淀粉溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
对处于平衡状态的反应2A(g)+B(g) 2C(g) △H<0,下
2C(g) △H<0,下
列叙述正确的是
A.增大A浓度的瞬间,V正 增大,V逆不变 B.升高温度,V正 减小,V逆增大
C.增大压强. V正 增大,V逆 减小 D.加入催化剂,V正、V逆 都增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com