
| A. | 裂化汽油可以用于萃取溴水中的溴 | |
| B. | 甘氨酸和丙氨酸缩合最多可形成4种二肽 | |
| C. | 盛放过苯酚的试剂瓶中残留的苯酚用酒精洗涤 | |
| D. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH |
分析 A.裂化汽油含碳碳双键;
B.氨基酸形成肽键原理为羧基提供-OH,氨基提供-H,两个氨基酸分子脱去一个水分子脱水结合形成二肽,既要考虑不同氨基酸分子间生成二肽,又要考虑同种氨基酸分子间形成二肽;
C.苯酚易溶于酒精;
D.酯化时羧酸脱羟基、醇脱H.
解答 解:A.裂化汽油含碳碳双键,与溴水发生加成反应,则不能萃取溴水中的溴,故A错误;
B.当同种氨基酸脱水,生成2种二肽;当是异种氨基酸脱水:可以是甘氨酸脱去羟基,丙氨酸脱氢;也可以丙氨酸脱羟基,甘氨酸脱去氢,生成2种二肽,共4种,故B正确;
C.苯酚易溶于酒精,则盛放过苯酚的试剂瓶中残留的苯酚用酒精洗涤,故C正确;
D.酯化时羧酸脱羟基、醇脱H,则在酸性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH,故D正确;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物官能团与性质的关系、有机反应为解答的关键,侧重烯烃性质的考查,注意选项A为易错点,题目难度不大.


 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:选择题
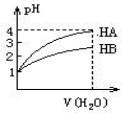 常温时,pH=1的两种一元酸HA和HB溶液,分别加水稀释1000倍,两溶液的pH与所加水的体积变化如图所示,下列结论中正确的是( )
常温时,pH=1的两种一元酸HA和HB溶液,分别加水稀释1000倍,两溶液的pH与所加水的体积变化如图所示,下列结论中正确的是( )| A. | 在稀释过程中当两者pH分别都是2时,c(HA)>c(HB) | |
| B. | 当稀释100倍时,HB溶液的pH=2 | |
| C. | 在稀释过程中HA与HB溶液中c(OH-)均增大 | |
| D. | 等体积pH=1的HA和HB溶液分别用等物质的量浓度的NaOH溶液中和,消耗碱溶液体积HA等于HB |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大压强.V正增大,V逆减小 | |
| B. | 升高温度,V正减小,V逆增大 | |
| C. | 增大A浓度的瞬间,V正增大,V逆不变 | |
| D. | 增大A浓度瞬间,V正增大而V逆减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a-b}{V}$ mol•L-1 | B. | $\frac{2a-b}{V}$ mol•L-1 | C. | $\frac{2(a-b)}{V}$ mol•L-1 | D. | $\frac{2(2a-b)}{V}$ mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粗盐提纯时,为了加快过滤速率,可以用玻璃棒进行搅拌 | |
| B. | 分液操作中,将下层液体放入烧杯中,再将上层液体继续放入另一烧杯中 | |
| C. | 测定硫酸铜晶体结晶水含量时,加热后的坩埚须在干燥器中冷却,再称量 | |
| D. | 蒸馏操作中,温度计水银球部位要插入液面下且不接触蒸馏烧瓶瓶壁 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com