
下表为周期表的一部分,其中的编号代表对应的元素。试填空。

(1)元素A分别与E、F、G形成最简单的常见化合物分子甲、乙和丙。下列有关叙述不正确的有________。
A.甲、乙和丙分子均为由极性键构成的极性分子
B.甲、乙和丙分子中,中心原子均采取sp3的杂化方式
C.三种分子中键角由大到小的顺序是甲>乙>丙
D.甲、乙和丙分子的空间构型分别为正四面体形、三角锥形、V形
(2)元素B基态原子中电子共占据了 个轨道,其价电子排布式为 。
(3)工业上制取D的单质时,并不采取电解D与I的化合物的方法,原因是 。
(4)在测定A与H形成的化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是________________________________________________。
(5)化合物CI3的溶液贮存较长时间,往往出现浑浊,原因是 (用离子方程式表示)。
(6)化合物(EF)2的性质与卤素单质相似,根据共价键理论推测,该分子中σ键和π键数目之比为________________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列平衡体系在体积不变时加入所给物质,平衡可以发生移动的是
A.FeCl3(aq)+KSCN(aq)  Fe(SCN)3(aq)+3KCl(aq),加入KCl晶体
Fe(SCN)3(aq)+3KCl(aq),加入KCl晶体
B.N2(g)+3H2(g)  2NH3(g),通入HCl气体
2NH3(g),通入HCl气体
C.CaCO3(s)  CaO(s)+CO2(g),加入CaCO3
CaO(s)+CO2(g),加入CaCO3
D.2SO2(g)+O2(g)  2SO3(g),通入N2
2SO3(g),通入N2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中的分子之间能形成氢键,且表示方法正确的是( )
A. H2O: H—O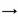 H B. H2S: H—S…H
H B. H2S: H—S…H
C. HCHO: C=O…H D. NH3: N—H…N
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关晶体的说法中一定正确的是( )
①依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体; ②由原子直接构成的晶体就是原子晶体; ③分子晶体的堆积均采取分子密堆积 ;④NaF、MgF2 、SiF4三种晶体的熔点依次升高;⑤金属键只存在于金属晶体中; ⑥离子键只存在于离子晶体中; ⑦H2O的性质非常稳定,原因在于分子之间存在氢键; ⑧SO2和SiO2晶体在熔化时破坏的作用力相同
A.①⑤⑥⑦ B.只有⑥ C.②③⑤⑥ D.①②⑤⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)铝在自然界中有游离态和化合态两种形式 ( )
(2)Mg、Al在空气中性质稳定,因而都具有很强的抗腐蚀性 ( )
(3)MgO与Al粉的混合物也可称为铝热剂 ( )
(4)Mg是活泼金属,而Al是两性金属 ( )
查看答案和解析>>
科目:高中化学 来源: 题型:
铝是中学化学学习阶段的唯一一种既能与酸(非氧化性酸)反应又能与强碱溶液反应放出H2的金属,就铝的这一特殊性质回答下列问题:
(1)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,所得H2的体积之比是________。
(2)足量的两份铝分别投入到等体积、等物质的量浓度的盐酸、氢氧化钠溶液中,产生H2的体积之比是________。
(3)足量的两份铝分别投入到等体积、一定物质的量浓度的HCl、NaOH溶液中,二者产生的H2相等,则HCl和NaOH的物质的量浓度之比是________。
(4)甲、乙两烧杯中各盛有100 mL 3 mol·L-1的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后,测得生成的气体体积比为V(甲)∶V(乙)=1∶2,则加入铝粉的质量为 ( )
A.5.4 g B.3.6 g C.2.7 g D.1.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
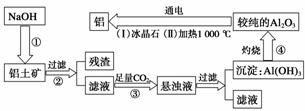
铝是地壳中含量最多的金属元素,在自然界主要以化合态形式存在于氧化铝中。铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质,冶炼金属铝很重要的一个过程是Al2O3的提纯。由于Al2O3是两性氧化物,而杂质SiO2是酸性氧化物,Fe2O3是碱性氧化物,因而可设计出两 种提纯氧化铝的方案。
种提纯氧化铝的方案。
方案一:碱溶法
讨论回答下列问题:
(1)写出①、③两步骤中可能发生反应的 离子方程式。
离子方程式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com