
A、苯的分子式为  |
B、HF的形成过程 |
C、四氯化碳的电子式  |
D、硫离子结构示意图  |
 .
. ,故B错误;
,故B错误;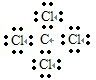 ,故C错误;
,故C错误; ,故D正确.
,故D正确.

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:
 某实验B小组测定金属锡合金样品的纯度(仅含少量锌和铜,组成均匀),将样品溶于足量盐酸:Sn+2HCl=SnCl2+H2↑,过滤,洗涤.将滤液和洗涤液合并再加过量的
某实验B小组测定金属锡合金样品的纯度(仅含少量锌和铜,组成均匀),将样品溶于足量盐酸:Sn+2HCl=SnCl2+H2↑,过滤,洗涤.将滤液和洗涤液合并再加过量的查看答案和解析>>
科目:高中化学 来源: 题型:

| A、Cl2+2KBr═Br2+2KCl |
| B、2NaHCO3?Na2CO3+H2O+CO2 |
| C、4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
| D、2Na2O2+2CO2═2Na2CO3+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、电解初期,石墨电极上有H2产生 | ||||
| B、整个电解过程中,H+的浓度不断增大 | ||||
| C、电解一定时间后,石墨电极上有铜析出 | ||||
D、电解初期,总反应方程式为:Cu+H2SO4
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 向某钾盐中加入澄清石灰水 | 有白色沉淀生成 | 该钾盐是K2CO3 |
| B | 在酸性KMnO4溶液中通入SO2 | 酸性KMnO4溶液褪色 | SO2具有漂白性 |
| C | 向溶液X中先滴加稀硝酸,再滴加硝酸钡溶液 | 出现白色沉淀 | 溶液X中一定含有SO42- |
| D | 向装有Fe(NO3)2溶液的试管中加入稀硫酸 | 在管口看到红棕色气体 | 氧化还原生成NO被氧化成NO2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4 L H2O含有的分子数为 NA |
| B、常温常压下,1.70g NaNO3含有的Na+离子数为0.02 NA |
| C、通常状况下,0.5 NA 个CO分子占有的体积为11.2 L |
| D、物质的量浓度为0.5mol?L-1的MgBr2溶液中,含有Br-个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、室温下,该溶液的pH=7 |
| B、适当加热该溶液,溶液的PH值升高 |
| C、c(Na+)>c(A-)>c(H+)>c(OH-) |
| D、c(Na+)+c(H+)=c(A-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCO3的电离方程式:CaCO3=Ca2++CO32- |
| B、HCO3-的电离方程式:HCO3-+H2O═H3O++CO32- |
| C、CO32-的水解方程式:CO32-+2H2O═H2CO3+2OH- |
| D、CaCO3的沉淀溶解平衡表达式:CaCO3(s)=Ca2+(aq)+CO32-(aq) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com