
| A. | W与X形成的两种化合物中阴、阳离子的个数比均为1:2 | |
| B. | Y、R、Z最高价氧化物对应水化物的酸性强弱顺序:Z>R>Y | |
| C. | W的简单氢化物稳定性比Z的简单氢化物稳定性低 | |
| D. | Y与W形成的化合物YW2的熔点高、硬度大 |
分析 R、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色,则X为Na元素;R元素的原子最外层电子数是其内层电子数的2倍,R元素原子有2个电子层,最外层电子数为4,故R为碳元素;W、Z同主族,Z的核电荷数是W的2倍,故Z为硫元素,W为氧元素;Y是地壳中除氧外含量最多的非金属元素,则Y为Si元素,据此进行解答.
解答 解:R、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色,则X为Na元素;R元素的原子最外层电子数是其内层电子数的2倍,R元素原子有2个电子层,最外层电子数为4,故R为碳元素;W、Z同主族,Z的核电荷数是W的2倍,故Z为硫元素,W为氧元素;Y是地壳中除氧外含量最多的非金属元素,则Y为Si元素.
A.W与X形成的两种化合物分别为Na2O,Na2O2,其中阴、阳离子的个数比均为1:2,故A正确;
B.Y、R、Z最高价氧化物对应水化物分别为H2SiO3、H2CO3、H2SO4,酸性强弱为:H2SO4>H2CO3>H2SiO3,故B正确;
C.W的氢化物为H2O,Z的氢化物为H2S,非金属性O大于S,则温度下H2O>H2S,故C错误;
D.Y与R形成的化合物YR为SiC,俗名为金刚砂,熔点高、硬度大,故D正确;
故选C.
点评 本题考查结构性质位置关系应用,题目难度不大,推断元素是解题的关键,注意对元素周期律知识的理解掌握,试题培养了学生的分析能力及灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:H2O>HF>H2S | B. | 酸性:H3PO4>H2SO4>HClO4 | ||
| C. | 原子半径:Na>Mg>O | D. | 氧化性:N2>Br2>Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、HCO3-、[Al(OH)4]- | ||
| C. | NO3-、Ca2+、K+、Fe2+ | D. | NO3-、K+、[Al(OH)4]-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠与硫酸氢钠反应 | B. | 碳酸钾溶液与稀盐酸反应 | ||
| C. | 苏打溶液与稀硝酸反应 | D. | 小苏打溶液与稀硫酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该铜铂电池属于二次电池 | |
| B. | 电子移动方向与纳米发动机移动方向相同 | |
| C. | 铜为铜柏电池的正极 | |
| D. | 铂极发生的电极反应为HBrO+H++2e-=Br-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
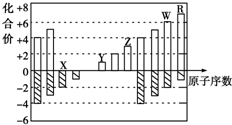 如下图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )
如下图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是( )| A. | 气态氢化物的稳定性:R>W | |
| B. | X与Y可以形成原子个数比为1:1和1:2的两种离子化合物 | |
| C. | 由X、Y、Z、W、R五种元素形成的简单离子中半径最小的是X2- | |
| D. | Y和Z两者最高价氧化物对应的水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 乙酸乙酯和水,酒精和水,苯酚和水 | |
| B. | 二溴乙烷和水,溴苯和水,硝基苯和水 | |
| C. | 甘油和水,乙醛和水,乙酸和乙醇 | |
| D. | 油酸和水,甲苯和水,己烷和水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 构成单质分子的微粒一定含有共价键 | |
| B. | 由非金属元素组成的化合物不一定是共价化合物 | |
| C. | 金属和非金属化合时一定形成离子键 | |
| D. | 含有共价键的化合物都是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过渡元素包括七个副族和第Ⅷ族的元素 | |
| B. | 第3列中元素种类最多 | |
| C. | 第17列的第一种元素对应最高价氧化物的水化物是最强的含氧酸 | |
| D. | 第15列元素的氢化物组成通式可用RH3表示 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com