
| A、胶体与溶液的分离可采用过滤的方法 |
| B、胶体与溶液的本质区别是有丁达尔效应 |
| C、将饱和氯化铁溶液滴入稀氢氧化钠溶液中加热,可得氢氧化铁胶体 |
| D、胶体属于介稳体系 |


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
| A、烷烃能使酸性KMnO4溶液褪色 |
| B、苯环能使KMnO4酸性溶液褪色 |
| C、苯环使甲基的活性增强而导致的 |
| D、甲基使苯环的活性增强而导致的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
| A、容器①、②中反应达平衡时,状态完全相同 |
| B、①平衡时,N2的转化率为25% |
| C、容器②中达平衡时放出的热量Q<23.15 kJ |
| D、若向容器①加入2molN2、6molH2,则平衡时放出的热量23.15kJ<Q1<46.3 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
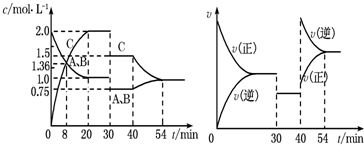
| A、30 min~40 min间该反应使用了催化剂 |
| B、反应方程式中的x=1,正反应为吸热反应 |
| C、30 min时降低温度,40 min时升高温度 |
| D、8 min前A的平均反应速率为0.08 mol?L-1?min-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强电解质溶液的导电能力一定强于弱电解质溶液 |
| B、乙酸溶液中存在的微粒有CH3COOH、CH3COO-、H+、OH-、H2O |
| C、0.05mol的NaOH固体分别加入到体积都是100ml的自来水、0.5mol/L的乙酸、0.5mol/L的盐酸和0.5mol/L的NaCl溶液中,溶液导电能力变化最小的是自来水 |
| D、在相同温度下,a强电解质,b弱电解质,c金属Al的导电能力相同,升高温度后它们的导电能力都增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol聚乙烯含有的原子数目为6NA |
| B、标况下1L己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA/22.4 |
| C、1 mol甲基含9NA个电子 |
| D、2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com