
向20mL盐酸和硫酸的混合酸溶液中,渐渐加入
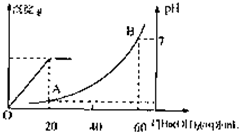
0.1mol/L的Ba(OH)2溶液。生成沉淀的质量和溶液的pH变化曲线如右图。根据此实验数据计算:

(1)原溶液中硫酸和盐酸的浓度各为多少_________________。
(2)A点处溶液的pH是______________。
(1)c(H2SO4)=0.1mol/L c(HCl)=0.4mol/L
(2) pH=0.7
本题以图示形式检查酸、碱中和生成沉淀质量和溶液pH曲线随加入Ba(OH)2溶液体积变化情况,此题属于理解层次的中等难度试题。
(1)依据图示,沉淀最大时已加入Ba(OH)2溶液20mL,混合酸中硫酸被完全中和。所以原混合酸中硫酸的物质的量浓度为0.1mol/L。
当H2SO4刚被Ba(OH)2溶液中和时,可以认为溶液中盐酸未被中和。从20mL起,再加Ba(OH)2溶液至60mL时溶液中盐酸全被中和完,溶液呈中性,pH=7,所以原混合酸中盐酸的物质的量浓度为0.4mol/L。
(2)A点处溶液中氢离子浓度是盐酸提供的,因H2SO4刚被Ba(OH)2溶液中和,溶液被冲稀,体积扩大到原来的2倍,则盐酸浓度缩小到原来的1/2,由原来的0.4mol/L变为0.2mol/L。即氢离子浓度为0.2mol/L。所以pH=0.7。


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
 室温时,盐酸和硫酸的混合溶液20mL,向混合物中逐滴加入0.05mol/L Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化).下列说法正确的是( )
室温时,盐酸和硫酸的混合溶液20mL,向混合物中逐滴加入0.05mol/L Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化).下列说法正确的是( )| A、图中A点溶液的pH=1 | B、生成沉淀的最大质量为2.33g | C、原混合溶液中盐酸物质的量浓度为0.1mol/L | D、当V[Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖北省武汉市高三二月调研测试理科综合化学试卷(解析版) 题型:选择题
室温时,盐酸和硫酸的混合溶液20mL,向混合物中逐滴加入0.05mol/L Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化)。下列说法正确的是

A.图中A点溶液的pH=1
B.生成沉淀的最大质量为2.33g
C.原混合溶液中盐酸物质的量浓度为0.1mol/L
D.当 [Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO
[Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO ═BaSO4↓
═BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
向20mL 盐酸和硫酸的混合溶液中,逐滴加入 0.1mol/L的 Ba(OH)2 溶液,沉淀的质量和溶液的pH值与加入的 Ba(OH)2 溶液体积的图像如下图所示(注意:起点时混酸的pH不为0)。回答:

(1)起始时,混合酸中硫酸的物质的量浓度是________mol/L,盐酸的物质的量浓度________mol/L。
(2)B点时沉淀的质量约是________g,
(3)A点时溶液中c(H+)为______mol/L;
(4)当酸碱恰好中和时,溶液中c(SO42-)为 mol/L。
已知Ksp(BaSO4)=1.1×10-10。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com