
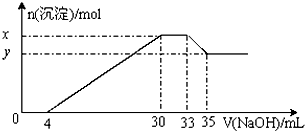
| A、原溶液中n(Mg2+):n(Al3+)=10:1 | B、原溶液中的c(H+)=0.8mol/L | C、x与y的差值为0.01mol | D、原溶液中c(Cl-)=0.66mol/L |
| 1 |
| 2 |
| 0.016mol |
| 0.2L |
| 0.132mol |
| 0.2L |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示.下列叙述正确的是( )
在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示.下列叙述正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
 (2011?金台区模拟)在200mL含Mg2+、Al3+、NH4+、H+、Cl- 等离子的溶液中,逐滴加入5mol?L-1NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.下列叙述不正确的是( )
(2011?金台区模拟)在200mL含Mg2+、Al3+、NH4+、H+、Cl- 等离子的溶液中,逐滴加入5mol?L-1NaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.下列叙述不正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
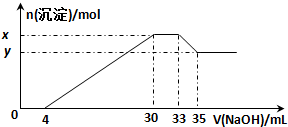 在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.
在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol?L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示.| A、x与y的差值为0.01 mol | B、原溶液中c(Cl-)=0.75 mol?L-1 | C、原溶液的pH=1 | D、原溶液中n(Mg2+):n(Al3+)=5:2 |
查看答案和解析>>
科目:高中化学 来源:2010届辽宁省大连协作体高二上学期竞赛(理综)化学部分 题型:选择题
在200mL含Mg2+、Al3+、、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示:
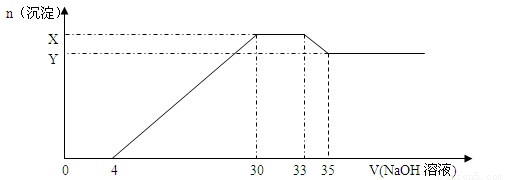
下列叙述正确的是
A. x与y的差值为0.02mol B.原溶液中c(Cl-)=0.825mol/L
C. 原溶液的PH=2 D原溶液中n(Mg2+):n(Al3+)=5:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com