
| A、1.5 g |
| B、3.0 g |
| C、4.2 g |
| D、9.0 g |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、2V酸=V碱 |
| B、V酸=2V碱 |
| C、V酸=102V碱 |
| D、102V酸=V碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/L |
| B、0.5 mol/L |
| C、0.01mol/L |
| D、0.05 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、正极 Zn 负极 Cu 电解质溶液 CuCl2 |
| B、正极Cu 负极Zn 电解质溶液 CuCl2 |
| C、正极Zn 负极Cu 电解质溶液 ZnCl2 |
| D、正极Cu 负极Zn 电解质溶液 ZnCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两种气体中含有相同的质子数 |
| B、SO2与CO2的密度之比为16:11 |
| C、SO2与CO2的质量之比为16:11 |
| D、SO2与CO2含有的电子数之比为16:11 |
查看答案和解析>>
科目:高中化学 来源: 题型:
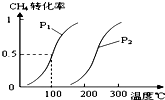 甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇.
甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇.| 实验编号 | T(℃) | n (CO)/n(H2) | P(MPa) | ||
| ⅰ | 150 |
| 0.1 | ||
| ⅱ | 5 | ||||
| ⅲ | 350 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com