
【题目】A、B、C、D、E、F为六种短周期主族元素,它们的原子序数依次增大;A元素的原子半径最小;B元素原子的最外层电子数是次外层电子数的3倍;C与A同主族,且与E同周期;E元素的最外层电子数是次外层电子数的0.75倍,D既可与C的最高价氧化物的水化物反应,也可与E的最高价氧化物的水化物反应,均有A元素的单质生成。请回答下列问题:
(1)写出F的元素名称_______________,元素B在周期表中的位置_______________。
(2)判断C、D、E离子半径的从大到小顺序________________,比较B和E的气态氢化物的稳定性大小______________________。
(3)写出单质D与C的最高价氧化物的水化物反应的离子方程式___________________。
(4)写出B与C按1:1形成化合物的电子式______________________,用电子式表示B与C按1:2形成化合物的过程_________________
(5)由A、B、C、E四种元素共同构成的两种化合物在溶液中相互间可发生化学反应,试写出该反应的离子方程式_____________________________。
【答案】 氯 第二周期第ⅥA族 S2— >Na+>Al3+ H2O>H2S 2Al+2OH-+2H2O=2 Al![]() +3H2↑
+3H2↑ ![]()
![]() HS
HS![]() +H+=H2O+SO2↑
+H+=H2O+SO2↑
【解析】A元素的原子半径最小,推出A为H元素;B元素原子的最外层电子数是次外层电子数的3倍,则B为8号O元素;C与A同主族,且与E同周期;E元素的最外层电子数是次外层电子数的0.75倍,则次外层一定是8个,最外层为6个,所以E为S元素,C为Na元素,D既与氢氧化钠反应、也与硫酸反应,均有氢气生成,所以D为Al元素。
(1)F的元素名称氯 ,O元素周期表中的位置第二周期第ⅥA族 。
(2)硫离子核外有3个电子层18个电子,所以其半径最大,而钠离子和铝离子都有10个核外电子,由于钠的核电荷数较小,其半径较大,所以离子半径的从大到小顺序为S2— >Na+>Al3+,O和S同一主族,O的非金属性较强,所以 O和S的气态氢化物的稳定性H2O>H2S。
(3)Al与氢氧化钠反应的离子方程式_2Al+2OH-+2H2O=2 Al![]() +3H2↑。
+3H2↑。
(4)写出B与C按1:1形成化合物的电子式![]() ,用电子式表示O与Na按1:2形成化合物的过程为
,用电子式表示O与Na按1:2形成化合物的过程为 ![]() 。
。
(5)由A、B、C、E四种元素共同构成的两种化合物分别为亚硫酸氢钠和硫酸氢钠,它们在溶液中相互间发生化学反应的离子方程式为HS![]() +H+=H2O+SO2↑。
+H+=H2O+SO2↑。


科目:高中化学 来源: 题型:
【题目】有机高分子材料M其结构简式为![]() ,下图是由有机物A(分子式为C5H8O)和苯甲醛为原料生产该有机物的合成路线。
,下图是由有机物A(分子式为C5H8O)和苯甲醛为原料生产该有机物的合成路线。

已知:① A分子中有两种不同环境的氢原子
② CH3CH2CH=CH2 ![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2
CH3CHO+ CH3CHO ![]()
![]()
请回答以下问题:
(1)A的结构简式为_____,B 的名称为_____,F中所含官能团的名称是______。
(2)①和③的反应类型分别是_______、______;反应② 的反应条件为_______。
(3)反应④的化学方程式为______________。
(4)有机物E有多种同分异构体,其中同时符合下列条件的同分异构体有_____________种。
① 属于芳香酯类 ② 其酸性水解产物遇FeC13 显紫色
(5)以l-丙醇和NBS为原料可以制备聚丙烯醇(![]() )。请设计合成路线(其他无机原料任选)并用如下方式表示:__________________
)。请设计合成路线(其他无机原料任选)并用如下方式表示:__________________
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A. 图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B. 图乙表示0.1LpH=2的HC1溶液加水稀释至VL, pH随lgV的变化
C. 图丙表示不同温度下水溶液中H+和OH-浓度变化的曲线,图中温度T2>T1
D. 图丁表示同一温度下,再不同容积的容器中进行反应2BaO2(s)![]() 2BaO(S)+O2(g),O2的平衡浓度与容器容积的关系
2BaO(S)+O2(g),O2的平衡浓度与容器容积的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+3B(g) ![]() 2C(g)+D(g) 在四种不同情况下的反应速率如下,其中反应进行得最快的是
2C(g)+D(g) 在四种不同情况下的反应速率如下,其中反应进行得最快的是
A.VA=0.15mol(Lmin)﹣1 B.VB=0.6 mol(Lmin)﹣1
C.VC=0.4 mol(Lmin)﹣1 D.VD=0.01 mol(Ls)﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂—磷酸氧铜电池正极的的活性物质是Cu4O(PO4)2,可通过下列反应制备:2Na3PO4+CuSO4+2NH3H2O═Cu4O(PO)2↓+3Na2SO4+(NH4)2SO4+H2O
(1)写出基态Cu2+的电子排布式:____________;与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有____________(填元素符号)。
(2)PO43-的空间构型是____________。
(3)P、S元素第一电离能大小关系为__________________,原因为__________________。
(4)NH3·H2O分子中NH3与H2O之间氢键表示为____________。(填序号)
A.N-H…O B.O-H…N C.H-N…H D.H-O…H
(5)氨基乙酸铜分子结构如图,碳原子的杂化方式为____________,基态碳原子核外电子有____________个空间运动状态。
![]()
(6)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则1mol该配合物中含有的π键的数目为______________。
(7)铜晶体为面心立方最密堆积,配位数为_______________,铜的原子半径为127.8pm,NA表示阿伏伽德罗常数的值,列出晶体铜的密度计算式______________g/cm-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关能量转换的说法正确的是 ( )
A.煤燃烧是化学能全部转化为热能的过程
B.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能
C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是一种重要的元素,其对应化合物在生产生活中有重要的应用。
(1)氮化铝(AlN)可用于制备耐高温的结构陶瓷,遇强碱会腐蚀,写出AlN与氢氧化钠溶液反应的离子方程式_______________。
(2)氨是制备氮肥、硝酸等的重要原料②③
①己知:N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
N2(g)+O2(g) ![]() 2NO(g) △H=+180 kJ/mol
2NO(g) △H=+180 kJ/mol
2H2(g)+O2(g) ![]() 2H2O(1) △H= -571.6 kJ/mol
2H2O(1) △H= -571.6 kJ/mol
试写出表示氨的标准燃烧热的热化学方程式________________。
②某电解法制氨的装置如右图所示,电解质只允许质子通过,试写出阴极的电极反应式__________。

(3)反应:2NO(g)+O2(g)![]() 2NO2(g)△H<0是制备硝酸过程中的一个反应。
2NO2(g)△H<0是制备硝酸过程中的一个反应。
①将NO和O2按物质的量之比为2:1置于恒温恒容密闭容器中进行上述反应,得到NO2体积分数与时间的关系如下图所示。保持其它条件不变,t1时再向容器中充入适量物质的量之比为2:1的NO和O2的混合气体,t2时再次达到平衡,请画出tl-t3时间范围内NO2体积分数随时间的变化曲线:____________。

②在研究此反应速率与温度的关系时发现,NO转化成NO2的速率随温度升高反而减慢。进一步研究发现,上述反应实际是分两步进行的:
I 2NO(g) ![]() N2O2(g) △H<0
N2O2(g) △H<0
II N2O2(g)+O2(g) ![]() 2NO2(g) △H<0
2NO2(g) △H<0
已知反应I能快速进行,试结合影响化学反应速率的因素和平衡移动理论分析,随温度升高,NO转化成NO2的速率减慢的可能原因________。
(4)已知常温下,Ka(CH3COOH)=Kb(NH3·H2O)=l.8×l0-5。则常温下0.lmol/L的CH3COONH4溶液中,(CH3COO-):c(NH3·H2O)=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某50 mL溶液中可能含有H+、Na+、Mg2+、Al3+、SO42-、NH4+离子,当向该溶液中加入5 mol/L的NaOH溶液时,发现生成沉淀的物质的量n(沉淀)随NaOH溶液的体积v(NaOH)变化关系如下图所示。
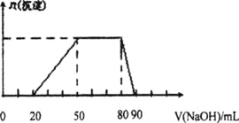
A.原溶液中一定含有的阳离子是H+、Mg2+、Al3+、SO42-
B. 原溶液中Al3+的浓度为lmol/L
C. 原溶液中NH4+的物质的量为0.4 mol
D. 当加入的NaOH溶液的体积为90mL时,反应后溶液中的离子只有Na+和SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com