
【题目】25℃时,HCN溶液中CN-和HCN浓度所占分数(α)随pH变化的关系如图所示,下列表述正确的是( )
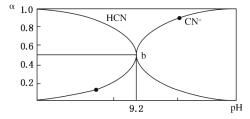
A.Ka(HCN)的数量级为10-9
B.0.1mol/LHCN溶液使甲基橙试液显红色
C.1L物质的量都是0.1mol的HCN和NaCN混合溶液中c(HCN)>c(CN-)
D.0.1mol/LNaCN溶液的pH=9.2
【答案】C
【解析】
A.电离平衡常数只受温度的影响,与浓度无关,取b点,c(HCN)=c(CN-),则有HCN的电离平衡常数表达式为Ka=![]() =c(H+)=10-9.2,Ka(HCN)的数量级约为10-10,故A错误;
=c(H+)=10-9.2,Ka(HCN)的数量级约为10-10,故A错误;
B. HCN为弱酸,其电离方程式为HCN![]() H++CN-,弱电解质的电离程度微弱,可以认为c(H+)=c(CN-),c(HCN)=0.1mol·L-1,根据电离平衡常数,0.1mol·L-1HCN溶液:
H++CN-,弱电解质的电离程度微弱,可以认为c(H+)=c(CN-),c(HCN)=0.1mol·L-1,根据电离平衡常数,0.1mol·L-1HCN溶液:![]() =10-10,解得c(H+)=10-5.5,即pH=5.5,甲基橙:当pH<3.1时变红,因此0.1mol·L-1HCN溶液不能使甲基橙显红色,故B错误;
=10-10,解得c(H+)=10-5.5,即pH=5.5,甲基橙:当pH<3.1时变红,因此0.1mol·L-1HCN溶液不能使甲基橙显红色,故B错误;
C. CN-水解平衡常数Kh=![]() =10-4>Ka=10-10,即CN-的水解大于HCN的电离,从而推出1L物质的量都是0.1mol的HCN和NaCN混合溶液中:c(CN-)<c(HCN),故C正确;
=10-4>Ka=10-10,即CN-的水解大于HCN的电离,从而推出1L物质的量都是0.1mol的HCN和NaCN混合溶液中:c(CN-)<c(HCN),故C正确;
D. 根据CN-水解平衡常数,得出:![]() =10-4,c(OH-)=10-2.5,pOH=2.5,则pH=11.5,故D错误;
=10-4,c(OH-)=10-2.5,pOH=2.5,则pH=11.5,故D错误;
答案:C。


科目:高中化学 来源: 题型:
【题目】(14分)溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
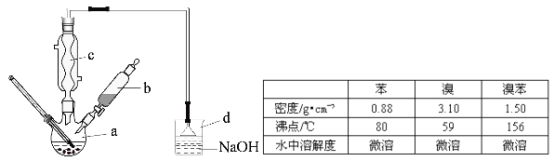
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了 气体。继续滴加至液溴滴完,装置d的作用是 ;
(2)液溴滴完后,经过下列步骤分析提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是 ③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤,加入氯化钙的是 ;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为 ,要进一步提纯,下列操作中必须的是 (填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)在该实验中,a的容积最适合的是 (填入正确选项前的字母)。
A.25mL B. 50mL C.250mL D.500mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验可以达到目的或得出结论的是( )
选项 | 实验目的或结论 | 实验过程 |
A | 探究浓硫酸的脱水性 | 向表面皿中加入少量胆矾,再加入约3mL浓硫酸,搅拌,观察实验现象 |
B | 相同温度下,Ksp(ZnS)<Ksp(CuS) | 向2mL ZnSO4 和CuSO4的混合溶液中逐滴加入0.01mol/L Na2S溶液,先出现白色沉淀 |
C | 淀粉已经完全水解 | 取少量酸催化后的淀粉水解液于试管中,先加入过量氢氧化钠溶液中和酸,再加少量碘水,溶液未变蓝 |
D |
| 向NaAlO2的试管中滴加碳酸氢钠溶液,产生白色沉淀 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取乙酸乙酯的装置。请回答:
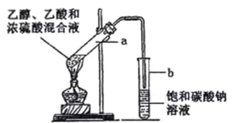
(1) 写出乙酸、乙醇酯化反应方程式__________
(2) 浓硫酸的作用是__________
(3) 下列有关该实验的说法中,正确的是__________
A.向 a 试管中加入沸石,其作用是防止加热时液体暴沸
B.饱和碳酸钠溶液可以除去产物中混有的乙酸
C.乙酸乙酯是一种无色透明、密度比水大的油状液体
D.若原料为 CH3COOH 和 CH3CH218OH,则乙酸乙酯中不含18O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用小粒径零价铁(ZVI)的电化学腐蚀处理三氯乙烯,进行水体修复的过程如图所示。H+,O2,NO3-等共存物的存在会影响水体修复效果,定义单位时间内ZVI释放电子的物质的量为nt,其中用于有效腐蚀的电子的物质的量为ne。下列说法错误的是( )
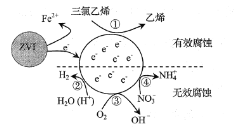
A. 反应①②③④均在正极发生
B. 单位时间内,三氯乙烯脱去amolCl时ne=amol
C. ④的电极反应式为NO3-+10H++8e-=NH4++3H2O
D. 增大单位体积水体中小粒径ZVI的投入量,可使nt增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2005年,全球发生了禽流感。我国科学家发现金丝桃素对高致病性禽流感病毒杀灭效果良好,某种金丝桃素的结构式如下图,下列有关金丝桃素说法错误的是
![]()
A. 分子式为C17H23NO3
B. 苯环上的一氯取代物有3种
C. 可以发生取代、加成、酯化等反应
D. 1mol金丝桃素最多能和4molH2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学或医学奖。青蒿素的一种化学合成方法的部分工艺流程如图所示:
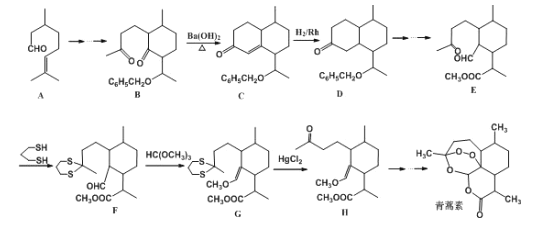
己知:①C6H5-表示苯基;②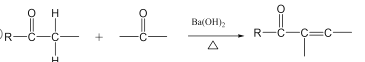
(1)化合物E中含有的含氧官能团有__、__和羰基(写名称)。
(2)合成路线中设计E→F、G→H的目的是__。
(3)B→C实际上是分两步反应进行的,先进行加成反应,再进行__反应。
(4)A在Sn-p沸石作用下,可生成同分异构体异蒲勒醇,己知异蒲勒醇分子中有3个手性碳原子(连有四个不同基团的碳原子称为手性碳原子),异蒲勒醇分子内脱水后再与H21:1发生1,4-加成可生成![]() ,则异蒲勒醇的结构简式为:__。
,则异蒲勒醇的结构简式为:__。
(5)A的同分异构体Y含有醛基和六元碳环,且环上只有一个支链,满足上述条件的Y有__种,其中核磁共振氢谱峰数最少的物质的结构简式为__。
(6)如图是以乙烯为原料制备苄基乙醛![]() 的合成路线流程图。
的合成路线流程图。
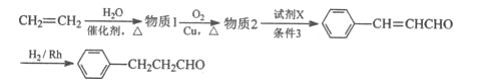
请填写下列空白(有机物写结构简式):
物质1为__;物质2为__;试剂X为__;条件3为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是学习化学的重要工具,它隐含着许多信息和规律。如图是元素周期表的一部分,表中所列序号①、②、③、④、⑤、⑥、⑦、⑧分别代表某种化学元素。根据表格所给信息,回答下列问题:
族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ||||||
3 | ⑤ | ⑥ | ⑦ | ④ | ⑧ | |||
(1)8种元素中,性质最稳定的是___(填元素符号)。
(2)①与④可形成___化合物(填“共价”、“离子”),其电子式为___。
(3)原子半径②___③,①___⑤(填“>”、“<”或“=”)。
(4)在元素⑤、⑥、⑦中,金属性最强的元素是___。(填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱,以及生产ClO2 和氯的含氧酸盐(NaClO、NaClO3)等系列化工产品。
(1)写出氯碱工业中电解饱和食盐水的离子方程式:________。
(2)①室温下,0.1 mol·L–1 NaClO溶液的pH___ 0.1 mol·L–1 Na2SO3溶液的pH。(填“大于”、“小于”或“等于”)已知:H2SO3的Ka1=1.54×10–2,Ka2=1.02×10–7;HClO的Ka=2.95×10–8
②写出一种可以证明NaHSO3溶液中HSO3–的电离程度大于HSO3–水解程度的方法:____
(3)氯气含量检测仪中,原电池工作原理示意图如图所示,则Cl2在Pt电极放电的电极反应为_____
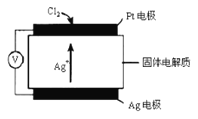
(4)工业上用NaClO3氧化酸性FeCl2废液,通过控制条件,使Fe3+水解产物聚合,形成可溶的多聚体,最终析出红棕色胶状沉淀Fe2O3·nH2O。其中水解形成羟桥配离子的离子方程式为:2Fe3++10H2O ![]() [Fe(H2O)4 (OH)2 Fe(H2O)4]4++2H+ 。欲使上述水解平衡正向移动,可采用的方法有________(填字母)。
[Fe(H2O)4 (OH)2 Fe(H2O)4]4++2H+ 。欲使上述水解平衡正向移动,可采用的方法有________(填字母)。
A.加水稀释 B.加热 C.加入盐酸 D.加入NaHCO3
(5)ClO2和Cl2均能将电镀废水中的CN– 氧化为无毒的物质,自身被还原为Cl–。处理含CN–相同量的电镀废水,所需Cl2的质量是ClO2的______ 倍。(保留三位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com